我们对血液肿瘤的基因变异多样性有哪些了解? 如何为科研和药物研发构建血液肿瘤模型?
血液肿瘤是怎么产生的?
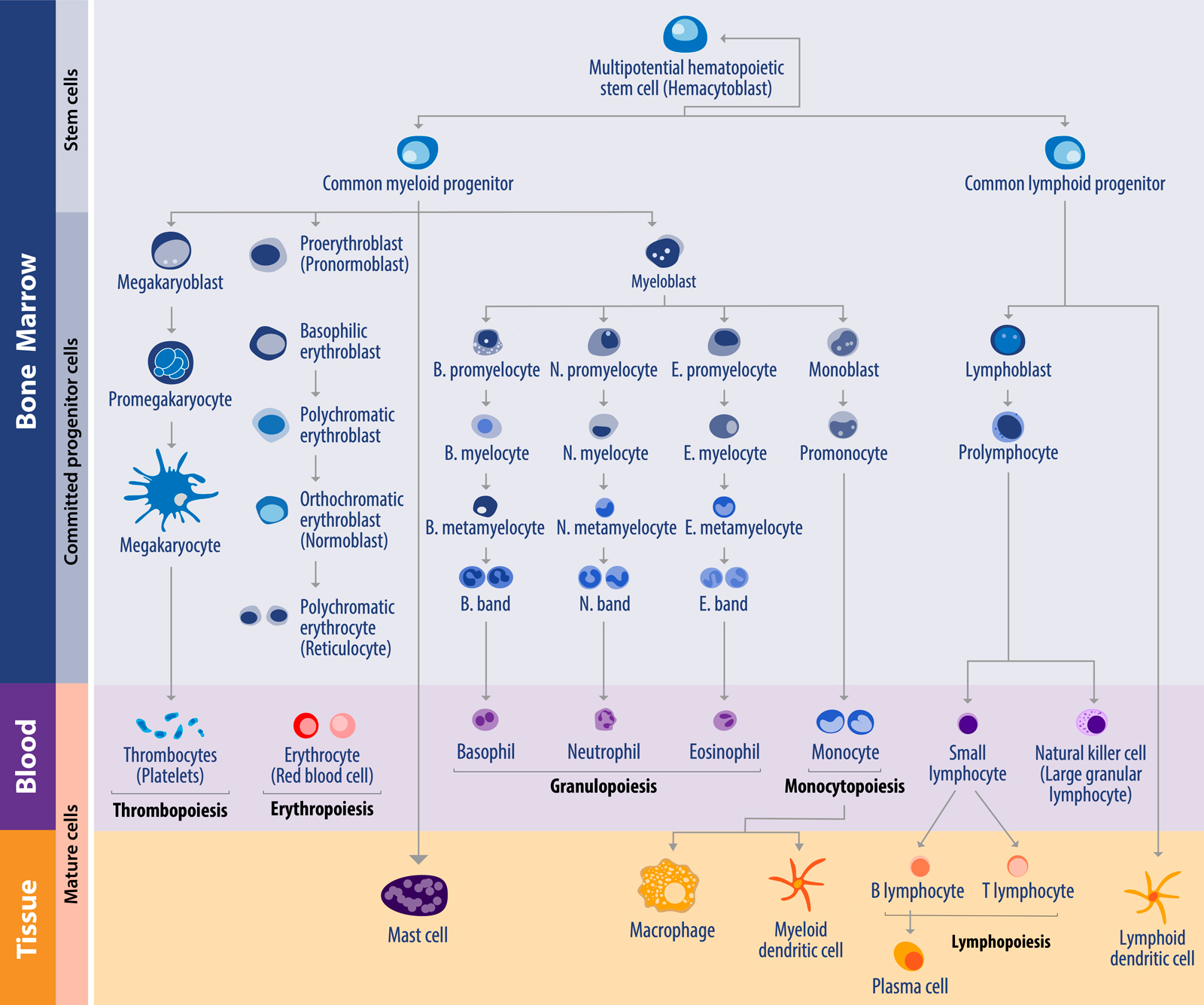
造血作用是一个动态发展的过程,骨髓中的造血干细胞(HSCs) 有自我更新和多向分化潜能,可终生贡献机体所需的各类血细胞。扰乱正常的造血分化过程就会导致血液肿瘤。血液肿瘤可被细分为三种主要类型:多发性骨髓瘤、白血病和淋巴瘤。
本文主要从不同血液肿瘤基因异常差异性,在研的血液肿瘤的靶向药物以及用于评估潜在新疗法的临床前血液肿瘤模型等三方面进行了综述。
多发性骨髓瘤(Multiple Myeloma, MM)
多发性骨髓瘤是一种在骨髓中的浆细胞异常增生的恶性疾病。浆细胞是构成人体免疫系统的成分之一。正常的浆细胞可产生抗体,发挥抗感染作用。浆细胞恶性增生后,在骨髓中积累,破坏或削弱骨骼,引起骨痛。恶性浆细胞还能产生异常抗体,改变体液免疫反应,增加感染的风险和影响抗感染的能力。
多发性骨髓瘤的病因目前尚不清楚,常伴有KRAS、NRAS、TP53、FAM46C、BRAF、DIS3、ATM和CCND1等基因的改变。这些基因的改变在多发性骨髓瘤的发病机制中发挥重要的作用,也为新的治疗方法提供了预测和治疗的靶点。
在过去的几十年里,多发性骨髓瘤的治疗方案有了很大的发展,包括:
- 化疗
- 糖皮质激素治疗
- 免疫调节剂 (thalidomide, lenalidomide, pomalidomide).
- 蛋白酶体抑制剂 (bortezomib, carfilzomib, ixazomib).
- 组蛋白脱乙酰基酶(HDAC)抑制剂 (panobinostat).
- 单克隆抗体 (daratumumab, elotuzumab).
白血病(Leukemia)
白血病是由于骨髓中异常白细胞的过度增生而引起的,并侵入周围血液循环。白血病根据白血病细胞种类及所占比例可分为急性淋巴细胞白血病(ALL)、急性髓细胞白血病(AML)、慢性淋巴细胞白血病(CLL)和慢性髓细胞白血病(CML)。其中,急性白血病发展较为迅速,需要及时采取积极治疗,以保证患者生命安全。
急性淋巴细胞白血病(ALL)
虽然大多数ALL的发病机制仍不清楚,但通常可观察到高频率的基因畸变。在B细胞ALL中,基因改变包括:
- 易位(如ETV6/RUNX1, BCR/ABL1, TCF3/PBX1).
- MLL 重排(包括11q23 及一系列伴侣基因).
- MYC重排到抗原受体基因位点.
- 肿瘤发生、肿瘤抑制、凋亡及细胞周期调节等相关基因突变 (如 CRLF2, IKZF1, TP53, and FLT3).
在T 细胞 ALL中, 常发生LYL1, TAL1, TLX1及 TLX3 基因重排.
成年ALL患者的主要治疗方法是长期联合化疗,包括对BCR-ABL重排患者使用酪氨酸激酶抑制剂靶向治疗(如imatinib, dasatinib, nilotinib, ponatinib, bosutinib)。
免疫疗法也可作为复发或难治性ALL的二线治疗方案。这包括针对CD19/CD3的双特异性抗体blinatumomab,针对CD22的单克隆抗体inotuzumab ozogamicin,或针对CD19的CAR-T细胞疗法tisagenlecleucel (Kymriah®)。放射治疗也可以在某些情况下使用。
急性髓细胞白血病(AML)
AML是一类遗传学高度异质性的疾病,其发病涉及多种染色体异常和基因突变。这些基因突变中与分化和预后最相关的是FLT3-ITD、NPM1、IDH1、IDH2和CEBPA基因突变。
大多数AML的主要治疗方法是化疗,通常使用阿糖胞苷或蒽环类药物。有时靶向治疗与化疗联合使用,如增加FLT3抑制剂(midostaurin, gilteritinib)或IDH抑制剂(ivosidenib, enasidenib)。
慢性淋巴细胞白血病(CLL)
在CLL中,TP53基因的状态对患者的预后及临床治疗选择具有重要的意义。此外,还包括NOTCH1、SF3B1、PO1、EGR2、MYD88、WNT通路以及缺失11q相关突变(ATM、BIRC3)。BTK和PLCG2的突变也在大约80%的ibrutinib 获得性耐药的CLL患者中发现。
治疗CLL的药物治疗种类繁多,例如:
- 化疗
- 放射治疗
- 针对CD20的单克隆抗体(rituximab, obinutuzumab, ofatumumab)
- 针对CD52的单克隆抗体(alemtuzumab)。
- 靶向CD22的重组免疫毒素(Lumoxiti™)
- BTK抑制剂(ibrutinib)
- PI3K抑制剂 (idelalisib, duvelisib)
- Bcl -2抑制剂 (venetoclax)
- 自体干细胞移植。
慢性髓细胞白血病(CML)
CML的发病机制主要是BCR-ABL基因重排。肿瘤抑癌基因和原癌基因(如p53、Rb1或Ras)相关的突变和染色体异常是白血病从慢性到急性进展所必需的。
由于CML患者存在BCR-ABL重排,所以使用酪氨酸激酶抑制剂 (imatinib, dasatinib, nilotinib, ponatinib, bosutinib)靶向治疗CML是标准治疗方法。化疗或干扰素治疗也常被用来治疗CML。
淋巴瘤(Lymphoma)
每年大约有一半的血液肿瘤新发患者是淋巴瘤或者淋巴系统肿瘤患者。淋巴瘤是由淋巴细胞(T细胞或B细胞)恶性增生而形成的。它们通过遍布全身的血液和淋巴系统循环转移到身体的许多部位,包括淋巴结、脾脏、骨髓和其他器官,造成损害。
淋巴瘤有几十种类型,主要的两大类是霍奇金淋巴瘤(HL)和非霍奇金淋巴瘤(NHL),二者约占90%的淋巴瘤。
HL的特征是Reed-Sternberg细胞的存在,该细胞是成熟的恶性B细胞。与之相比,NHL是由B细胞或T细胞衍生而来,可以出现在淋巴结和其他器官。
HL的预后和治疗方法各不相同,不同类型的NHL治疗方法也存在差异。在HL治疗中,除了常规的化疗或放疗外,还采用免疫治疗,如抗CD30的单克隆抗体 (brentuximab vedotin)、抗CD20抗体(rituximab)或抗PD-1的免疫检查点抑制剂(nivolumab, pembrolizumab)。
NHL的治疗方法与NL的相似,除了化疗或放射治疗外,还包括一些已经获批的免疫疗法:
- 抗CD30单克隆抗体抗 (brentuximab 及vedotin)
- 抗CD20抗体 (rituximab, obinutuzumab, ofatumumab 及ibritumomab tiuxetan)
- 抗CD52抗体 (alemtuzumab)
- PD-1免疫检查点抑制剂 (nivolumab, pembrolizumab)
- 免疫调节药物(thalidomide, lenalidomide)
- CD19 CAR-T疗法 (axicabtagene ciloleucel, tisagenlecleucel)
血液肿瘤药物临床前检测模型
为了更好理解血液肿瘤复杂的生物学特性以及评估潜在的新疗法或联合疗法,建立临床前转化医学模型是十分必要的。传统的血液肿瘤模型大多是细胞系来源的异种移植模型,多使用病人组织在体外构建永生的细胞系。
病人来源的异种移植(PDX)临床前血液肿瘤模型是从病人的血液中发展而来,这些模型不经过体外增殖直接植入小鼠体内,具有高度预测性的。为了建立这些血液肿瘤PDX模型,提取患者外周血或骨髓,接种到小鼠体内,构建原代模型。该模型可用于评估先导化合物的多种药理学特性(如PD、药效等)和研究疾病的表征和人群特异性。
尽管在开发此类模型上存在诸多挑战,但已有大量的血液肿瘤模型构建成功。例如,目前已有多种AML表型的模型构建成功,包括分化程度不高且局限于骨髓的模型,以及分化程度较高的PDX模型,这些肿瘤模型可侵入周围器官,并伴随脾脏肿大等特征。由于PDX模型能较好地反映患者肿瘤的组织病理学和分子病理学,为血液肿瘤的临床前药物评价提供了高度预测模型工具。
总结
血液肿瘤基因型和表型的多样性意味着需要大量的靶向药物、免疫疗法和联合治疗方案来对抗这种疾病,也需要建立临床前模型来捕捉临床疾病的多样性。PDX模型的出现为评估下一代血液肿瘤药物提供了前瞻性的选择。