开发能够最好地反映临床转移过程进展的临床前小鼠肿瘤模型。
转移性癌症的调查
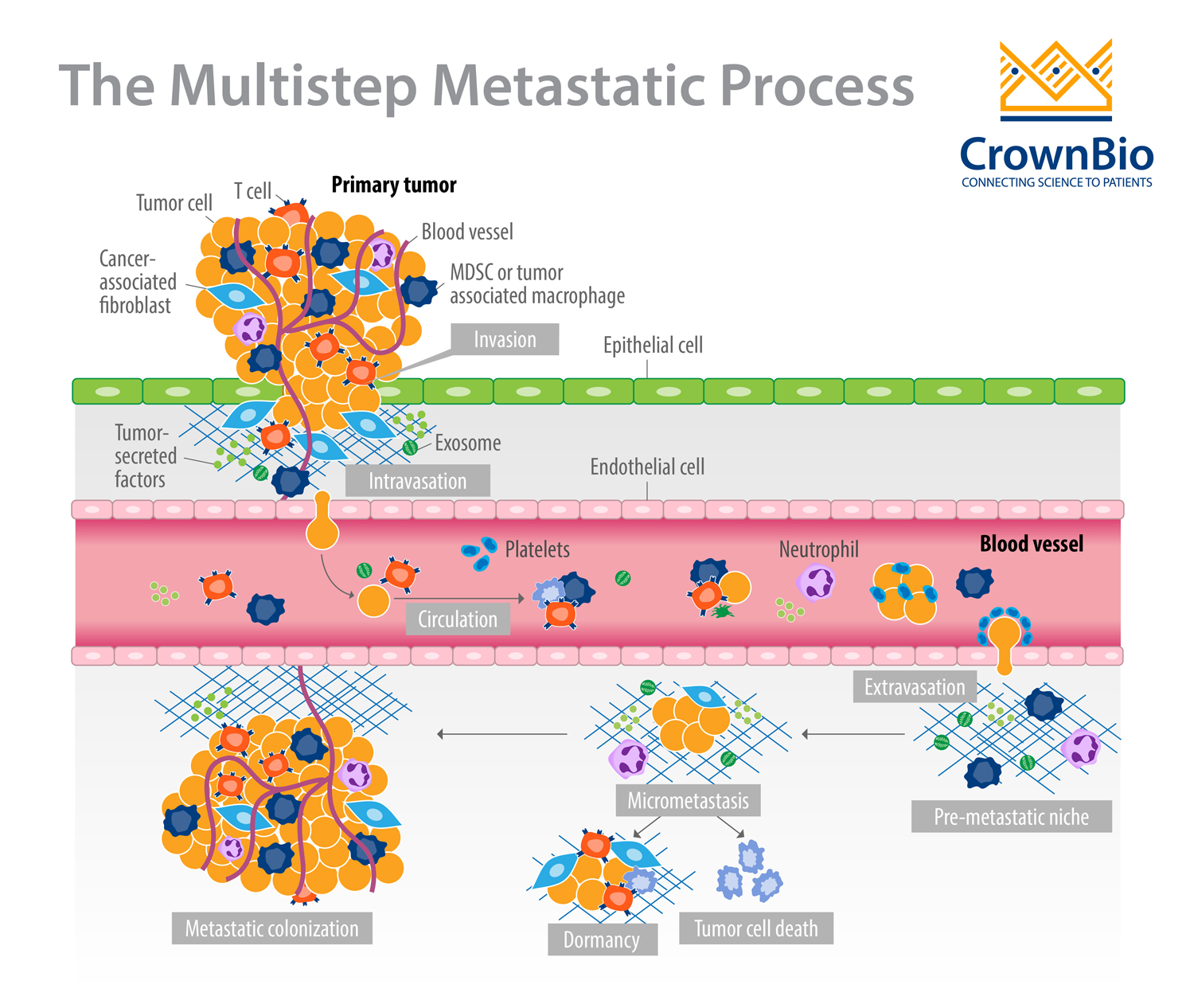
转移性癌症对患者具有破坏性的影响,并导致超过90%的癌症相关死亡。 转移的形成是一个非常低效的过程,是由一系列癌细胞发生的事件引起的:
- 从原发肿瘤部位迁移。
- 在淋巴系统或血管中存活。
- 从淋巴系统或者血管中渗出。
- 在远处生长以形成继发性肿瘤。
能够发生转移的原发性肿瘤的特性非常复杂,具体机制仍在研究之中。但是,目前被认为受到癌细胞内基因组改变(遗传和表观遗传)以及肿瘤微环境的高度影响。
肿瘤转移的临床前小鼠模型
临床前肿瘤学小鼠模型在提高我们对复杂相互作用和转移过程阶段的了解方面发挥着重要作用。改进的模型有助于研究人员更好地了解潜在的生物过程,并开发新的治疗方法来阻止转移或更有效地治疗已经确定的转移。
在临床前小鼠模型中有几种用于产生转移的方法,并且在选择转移模型时必须考虑各种因素。这些包括小鼠品系(包括其免疫状态),移植位置(例如皮下/异位,原位,静脉内),以及移植细胞的起源和类型(例如原代或永生化的人/小鼠癌细胞系,切除的患者肿瘤组织)。
细胞系来源的同源和异种移植模型较为常用,并且成功地用于模拟与各种类型的癌症相关的转移过程。例如:
- 同种移植:使用B16-F10细胞系的黑色素瘤和使用4T1细胞系的乳腺癌。
- 异种移植:使用MDA-MB-231细胞系的乳腺癌。
同系模型是在健全的小鼠免疫系统的背景下,而异种模型则处于免疫缺陷环境中。
在转移模型中具有明显优势的两种模型是基因工程小鼠模型和患者来源的原位异种移植模型。
使用基因工程小鼠模型(GEMMs)研究转移
使用GEMM发现转移的几个关键特征,包括转移可在肿瘤早期发生。先前认为转移仅发生肿瘤后期。
各种不同适应症的GEMMs可用于对转移过程进行建模。这些模型显示在免疫健全肿瘤微环境中的从头肿瘤进展和转移形成。这使得GEMMs成为非常适合用于研究细胞信号传导途径,肿瘤微环境和免疫应答的各种组分和功能作用的模型。
通过肿瘤的从头发展,GEMMs能够模拟肿瘤的细胞自主性的和基质对转移级联的所有阶段的影响。由于这个原因,允许在体细胞中有条件激活癌基因和/或抑制肿瘤抑制基因失活的模型反映了人类疾病的许多关键特征。
下面针对不同的癌症适应症详述这些模型的实例。
乳腺癌
MMTV-PyMT是用于研究乳腺肿瘤进展和转移的最常用的小鼠模型。 MMTV-PyMT转基因小鼠在小鼠乳腺肿瘤病毒启动子/增强子的转录控制下表达多瘤病毒中T抗原。该模型分享了在人类中看到的乳腺癌进展的许多方面,其特征是可以看到从增生到晚期癌的多阶段进展,随后是淋巴结和肺中的转移性病变。
前列腺癌
多种策略用来构建前列腺癌小鼠模型。最流行的模型之一是用于前列腺腺癌的的转基因小鼠前列腺癌(TRAMP)模型。 TRAMP模型基于probasin启动子调控SV40 T抗原癌蛋白表达。在淋巴结和肺中观察到远处转移,偶尔在骨,肾和肾上腺中观察到转移。
肺癌
用于诱导型肺癌发展的最常用的小鼠模型是LSL-KRASG12D模型。该模型含有激活形式的KRAS,由LoxP-Stop-LoxP(LSL)转录盒调节。
通过引入重组腺病毒诱导的Cre表达导致LSL转录终止盒的缺失,从而允许KRASG12D表达和肺腺癌的形成。 LSL-KRASG12D; Trp53flox/flox复合小鼠随后可以高频率地产生淋巴结,胸膜,肾脏,心脏,肾上腺和肝脏的转移。
胰腺癌
与肺腺癌模型类似,胰腺导管腺癌(PDAC)的许多模型依赖于LSL-KRASG12D小鼠来建立。 含有KrasG12D, Trp53R172H和Pdx-1Cre(称为KPC)的GEMMs小鼠模型反映了人胰腺癌的病理特征,其可以转移到多个器官,包括肝脏,淋巴结,肺,膈肌和肾上腺。
结肠癌
尽管开发了大量结肠癌GEMMs,但很少显示出高频率的转移效率。 以LSL-KRASG12V; APC flox/flox 小鼠为例; 在结肠中注射Cre腺病毒来诱导APC的丧失和致癌基因KRASG12V的激活,导致散发性肿瘤发展,随后产生肝转移。
患者来源的原位异种移植肿瘤模型(PDOX):更好地模仿患者肿瘤特性
可以将源自患者的异种移植物(PDXs)皮下或原位移植到免疫缺陷的受体小鼠中。它们通常是皮下模型,因为移植技术要求较低,并且可以有效监测肿瘤生长。
原位异种移植模型的优点
然而,丰富的经验表明,大多数皮下PDX模型不会发生转移。相反,患者来源的原位异种移植(PDOX)模型,其需要原位植入完整的肿瘤组织,可导致转移发生。这更能够接近人类肿瘤转移的真实倾向,并且可能更好地反映其潜在的转移过程。已经使用各种肿瘤类型成功建立了PDOX模型,包括胰腺,肺,乳腺和结肠。
原位植入的肿瘤也被证明在模仿相应的患者肿瘤的药物反应,肿瘤生长模式和转移特征(也见于此处)方面具有优越性,这可能是由于局部基质所赋予的重要影响。
原位异种移植模型的缺点
然而,原位移植可能更为耗时,并且在技术上更具挑战性。它还经常需要成像(例如超声,CT扫描)或探查性剖腹术来确认内部肿瘤的存在。有时,潜伏期很长,因此可能需要切除原发肿瘤才能使转移发生。
概要
转移性疾病对许多患者癌症具有破坏性的影响。 更好地反映全部转移过程的临床前小鼠模型更有可能产生可以用于患者的研究,从而改善其临床预后效果。
选择转移模型时应慎重考虑。 GEMMs为在免疫健全动物的转移模型的建立提供了有利条件,而原位PDX模型则显示出转移过程的更高保真度。