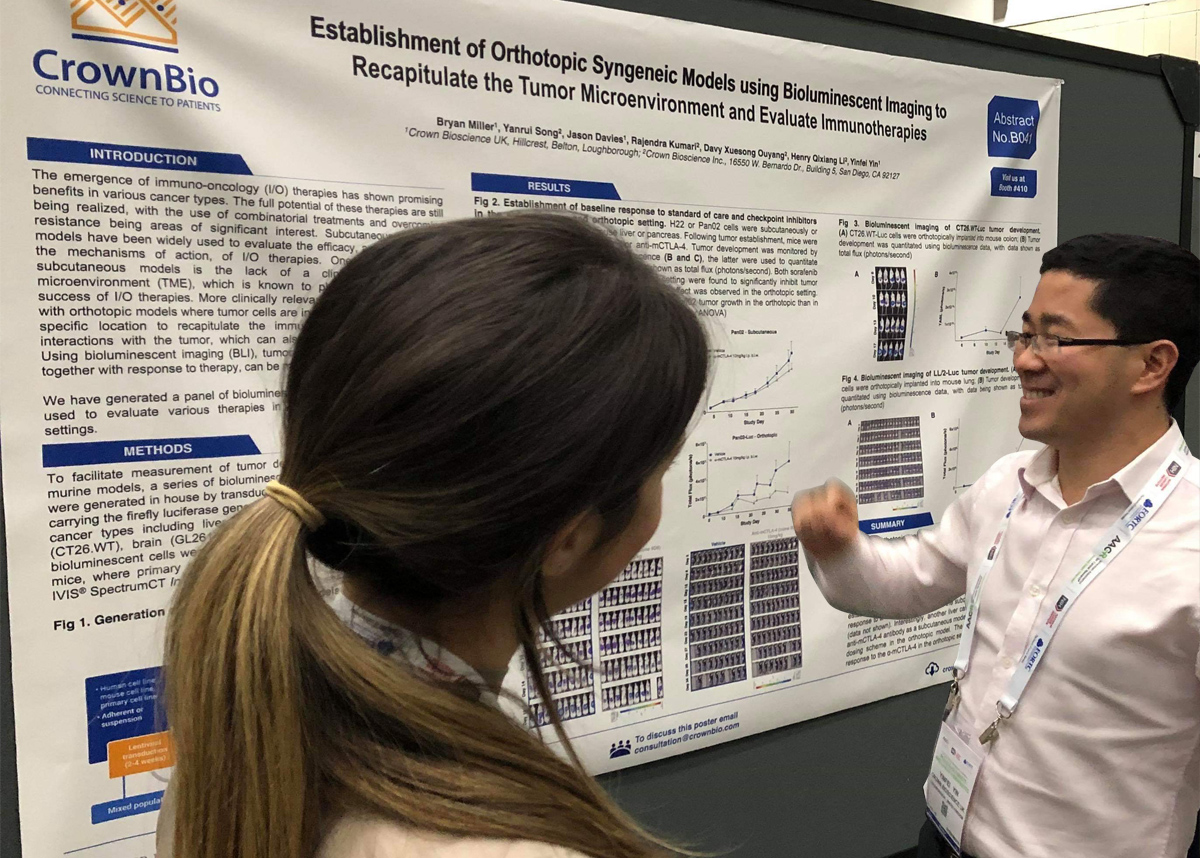
本周我们将在波士顿展示我们体内肿瘤模型小组的最新研究进展。了解我们在异种移植和同种移植模型成像、同种移植模型免疫原性改善以及PDX移植位点转录组分析方面的最新创新成果。
一系列系统性生物发光血液细胞衍生的异种移植模型的建立和应用(AACR-NCI-EORTC 2019,A009海报)
 我们的第一张成像海报介绍了血液恶性肿瘤建模的研究进展。目前该领域许多体内研究均采用皮下异种移植模型。然而,这种模型并不适用于骨髓及淋巴器官,也不适用于模拟癌症转移情况。
我们的第一张成像海报介绍了血液恶性肿瘤建模的研究进展。目前该领域许多体内研究均采用皮下异种移植模型。然而,这种模型并不适用于骨髓及淋巴器官,也不适用于模拟癌症转移情况。
在这两个前沿领域有所改善的模型是生物发光系统性异种移植模型。系统性移植模型能够更好地再现临床疾病,并可与成像技术结合,实时监测疾病进展和治疗反应。
生物发光系统性异种移植模型的建立与验证
在提供治疗数据之前,该海报首先展示了我们已为血液恶性肿瘤建立的生物发光系统性模型。我们的模型包括DLCBL模型(PD-L1过度表达的Raji,以及CD19、CD22和CD19/22敲除的Raji模型)、多发性骨髓瘤(MM.1S)以及白血病模型(MV4-11、Nalm6、MEC-1和CCRF-CEM)。所有模型均表达萤火虫荧光素酶,可被生物发光成像系统检测到。
这些模型的标准护理数据大多呈现良好的治疗反应。在MM.1S-Luc模型中,采用来那度胺治疗产生了显著的抗肿瘤反应;在Nalm6-Luc模型中,采用环磷酰胺和长春新碱亦引起了强烈的抗肿瘤反应。在Raji Luc模型中,利妥西单抗(Rituximab)虽能降低肿瘤负荷,但生存受益不显著。
我们还提供了针对Raji-Luc模型进行CD19 CAR-T细胞治疗的数据,CD19 CAR-T细胞治疗是血液恶性肿瘤治疗的一种重要的新方法。
我们正继续开发模型,建立更多的新模型,并持续进行特性鉴定,以期找到最佳的组合策略。
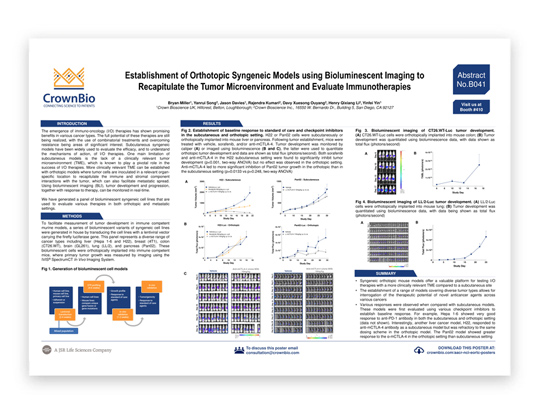
运用生物发光成像技术建立原位同种移植模型,再现肿瘤微环境并进行免疫治疗评价(AACR-NCI-EORTC 2019, B041)
 除建立生物发光异种移植模型外,我们也在创建生物发光
同种移植模型。这让我们可以进行模型的原位移植与监测,与皮下模型相比,肿瘤微环境(TME)更具有临床相关性。这对免疫肿瘤学研究非常重要,因为TME在免疫治疗反应中发挥着关键作用。原位同种移植也可再现免疫及基质成分与肿瘤的相互作用,这种相互作用可促进肿瘤转移扩散。
除建立生物发光异种移植模型外,我们也在创建生物发光
同种移植模型。这让我们可以进行模型的原位移植与监测,与皮下模型相比,肿瘤微环境(TME)更具有临床相关性。这对免疫肿瘤学研究非常重要,因为TME在免疫治疗反应中发挥着关键作用。原位同种移植也可再现免疫及基质成分与肿瘤的相互作用,这种相互作用可促进肿瘤转移扩散。
生物发光同种移植模型的建立与验证
我们已经建立了一系列表达萤火虫荧光素酶的同种移植模型,涉及多种癌症:
- 肝癌 — Hepa 1-6-Luc和H22-Luc。
- 乳腺癌 — 4T1-Luc。
- 结直肠癌 — CT26.WT-Luc。
- 脑癌 — GL261-Luc。
- 肺癌 — LL/2-Luc。
- 胰腺癌 — Pan02-Luc。
B041海报重点比较了皮下模型与原位模型的治疗反应。例如,尽管抗CTLA-4和索拉非尼对H22皮下模型有效,但相应的H22-Luc原位模型却对这两种治疗均具有耐药性。相反,对于Pan02模型,原位移植则可增强抗CTLA-4的治疗反应。
我们也详细介绍了肿瘤在一些结肠癌和肺癌新模型中的发展。
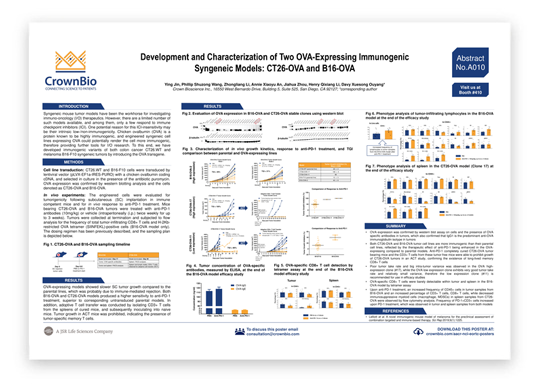
两种表达OVA的免疫原性同种移植模型 — CT26-OVA和B16-OVA的建立和表征(AACR-NCI-EORTC 2019,A010海报)
 我们的下一张海报将继续展示如何增强这些同种移植模型的免疫原性。可能由于固有的低/非免疫原性,其对免疫检查点抑制剂(ICI)的同系反应有限。
我们的下一张海报将继续展示如何增强这些同种移植模型的免疫原性。可能由于固有的低/非免疫原性,其对免疫检查点抑制剂(ICI)的同系反应有限。
为了改善这种情况,我们建立了表达卵清蛋白(OVA)的CT26.WT和B16-F10肿瘤模型。OVA具有高度免疫原性,而该海报探讨了OVA的表达是否会使同种移植模型更具免疫原性。
表达OVA的同种移植模型的建立与验证
建立稳定的CT26-OVA和B16-OVA克隆系,并通过western blot评价表达水平,从而筛选出OVA高、低表达的克隆系。然后,通过抗PD-1抗体对免疫原性进行评价。CT26-OVA和B16-OVA同种移植模型比其亲本细胞系表现出更高的免疫原性,且治疗反应增强。
抗PD-1治疗完全“治愈”了携带CT26-OVA肿瘤的小鼠,在一项过继细胞研究中,来自这些无肿瘤小鼠的CD3+T细胞抑制了CT26-OVA肿瘤的生长。这证明了CD8+T长寿记忆细胞的存在。
在疗效研究结束时,我们还对B16-OVA模型中的肿瘤浸润淋巴细胞和CT26-OVA模型中的脾脏进行了表型分析。 FACS分析显示,各种免疫细胞谱系或增加或减少。
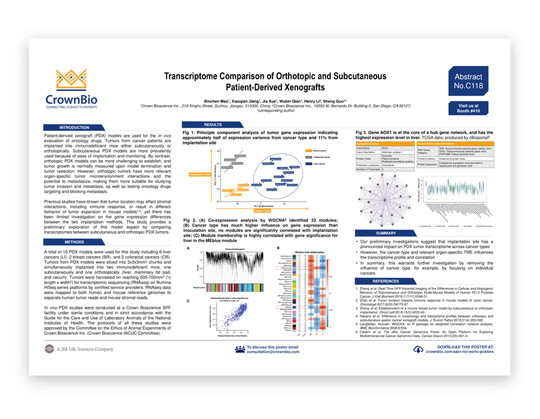
原位与皮下人源异种移植的转录组比较(AACR-NCI-EORTC,C118海报)
 如B041海报所示,肿瘤移植位点很重要。C118海报将其归因于人源异种移植(PDX)和基因表达。前期PDX研究表明,肿瘤的位置影响基质相互作用,包括免疫应答以及小鼠模型中的肿瘤扩增。然而,PDX中皮下和原位移植对基因表达的影响还有待深入的研究。
如B041海报所示,肿瘤移植位点很重要。C118海报将其归因于人源异种移植(PDX)和基因表达。前期PDX研究表明,肿瘤的位置影响基质相互作用,包括免疫应答以及小鼠模型中的肿瘤扩增。然而,PDX中皮下和原位移植对基因表达的影响还有待深入的研究。
C118海采用10个肝癌、乳腺癌和结直肠癌模型,比较了皮下和原位PDX肿瘤的转录组。使用了RNAseq进行转录组测序,将所得数据与人类和小鼠参考基因组进行比对,以分别读取人类肿瘤和小鼠基质。
我们的初步研究表明,移植位点显著影响不同癌症PDX肿瘤转录组。然而,癌症类型和相应器官特异性TME也会影响转录组谱和相关性。
为了增强我们的研究能力并巩固这些知识,接下来我们可能会关注癌症个体研究,最终消除癌症类型的影响。
阅读更多关于AACR-NCI-EORTC 2019的信息
阅读更多关于类器官和生物标志物发现平台的海报更新信息。