探索如何通过线性混合模型方法使用小鼠临床试验和分析来重新解读临床试验结果,包括失败的试验和生物标志物验证。
通过线性混合模型框架应用小鼠临床试验分析
与其他临床前研究相比,小鼠临床试验(MCT))是最大限度地模拟临床试验的群体、II期研究。使用几组PDX模型,MCT可提供高预测性的有效性数据,并提供有关缓解者/无缓解者人群的建议。
我们先前已经写过开发 线性混合模型(LMM)方法用于MCT分析的文章。这改进了当前基于终点的分析方法,并且有多种应用,包括指导MCT研究设计 和药物有效性/效应的准确定量。
LMM分析也可用于分析和重新解读临床结果,包括生物标志物验证。
使用MCT和LMM分析进行临床生物标志物验证
临床试验有时会产生相互矛盾的结果。MCT和LMM分析有助于更深入地挖掘数据并揭示实际趋势。一个很好的例子是针对临床试验中产生的潜在生物标志物。
针对ERCC1是否可预测胃癌患者对顺铂的反应,两项已发表的临床试验(Bamias et al和De Dosso et al)显示存在差异。尽管这两项试验的患者例数以及Kaplan-Meier生存分析的p值几乎相同。
已对一组PDX的MCT顺铂数据进行了LMM分析,以开始解决该问题。除了PDX组对顺铂的反应外,还通过RNAseq确定了ERCC1的表达水平。对于42个PDX(包括胃、肺和食管模型)的MCT组,ERCC1表达范围较广。
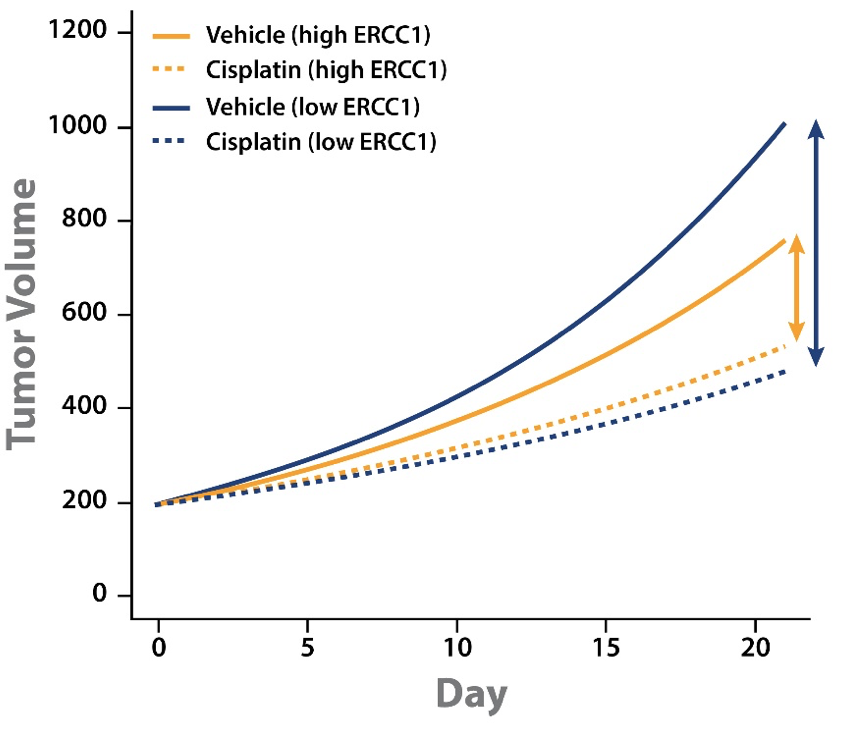
然后可以通过ERCC1高表达或低表达水平的模型分离肿瘤生长抑制(TGI)数据。该分析显示了一些有趣的点:
- 对于ERCC1高表达和低表达的PDX,顺铂治疗均可减缓肿瘤生长。
- 对于ERCC1高表达和低表达的PDX,溶媒组和顺铂组之间的幅度差异表明,顺铂对ERCC1低表达PDX的影响更大。
这种分析在某种程度上解释了相互矛盾的临床结果。ERCC1低表达水平的PDX肿瘤生长较快,并从顺铂治疗中获益。因此,ERCC1阴性患者将从顺铂治疗中获益更多,因此如果不治疗,预后更差。
顺铂治疗可改善其预后,但尚不清楚其总体预后是否优于ERCC1阳性患者。
应用MCT和LMM重新解读失败的临床试验
MCT的主要用途是在临床前环境中确定缓解者和无缓解者亚组,以改善临床中的患者分层。MCT和LMM分析也可用于重新评估失败的临床试验,以寻找仍可能从治疗中获益的特定患者亚组。
已知EGFR抑制剂西妥昔单抗可诱导EGFR高表达或拷贝数扩增的PDX中产生更大的反应。通过将EGFR表达与西妥昔单抗TGI数据相关联来确定这一点。
然而,使用基于终点的分析方法(如TGI)存在局限性。包括对计算天数、组间初始肿瘤体积差异和肿瘤生长率的依赖性。TGI与有效性的实际相关性较弱。然而,使用LMM模拟基因对肿瘤生长的影响时,LMM仍然表明EGFR是排名第一的基因。
在临床上,一项随机、III期、开放性试验观察了 西妥昔单抗联合卡培他滨-顺铂治疗晚期胃癌患者的获益。研究论文没有发现在该方案中加用、西妥昔单抗的额外益处。
然而,结果可以重新解读,特别是寻找EGFR蛋白表达评分高(>200)的患者。该研究发现试验中的29名患者,21名仅接受化疗,8名患者加用西妥昔单抗。从生存期结果来看,观察到加用西妥昔单抗存在明显差异:
- 单独化疗患者的中位PFS为4个月,加用西妥昔单抗的患者的中位PFS为8个月。
- 单独化疗患者的中位OS为10.1个月,加用西妥昔单抗的患者的中位OS为19.5个月。
对于这一独特的患者亚组,西妥昔单抗似乎确实提供了临床获益,将该亚组从失败的临床试验中拯救出来。
结论
小鼠临床试验和复杂的分析为评估相互矛盾的临床数据提供了解决方案,并对失败的临床试验进行了密切分析。对于潜在的生物标志物,MCT为标记物验证提供了理想的研究类型,允许衡量使用溶媒治疗的肿瘤生长。