探索如何将人源肿瘤类器官应用于临床中,从而开发出用于指导和推介治疗方案的新型精准医疗方法。
什么是人源肿瘤类器官?
人源肿瘤类器官是一种区域变革性临床前肿瘤模型系统。3D类器官直接来源于患者肿瘤组织,使用专门设计的培养条件来保存原发肿瘤的肿瘤干细胞(CSC)成分。因此,由于CSC能够自我更新并分化为原始肿瘤中可找到的多种细胞类型,所以类器官忠实再现了原发肿瘤的复杂性。
Hubrecht类器官技术(HUB)方案基于Clevers实验室首创的方法,是开发人源类器官肿瘤的先驱方案。这些方法利用了 多种生长因子,不借助饲养层细胞来生成稳健的肿瘤类器官,因而忠实再现了原始肿瘤的多个特性。.
肿瘤类器官再现原始肿瘤组织特征
人源肿瘤类器官涵盖CSC及其下游分化程度较高的子代。肿瘤类器官还拥有与原发肿瘤相同的基因组特征。例如,已证明胰腺肿瘤类器官可维持致癌基因改变(例如KRAS、TP53、SMAD、CDKN2A、扩增的MYC)以及肿瘤抑制基因TGFBR2和DCC的缺失。
肿瘤类器官也表现出与原发性肿瘤组织学相似的形态结构,例如胰腺、结肠、乳腺、前列腺、肺、肝等。这可能包括产生转移性肿瘤常见的侵袭表型。基因和蛋白表达也与相应原发肿瘤细胞亚型相似。
肿瘤类器官使精准医疗方法成为可能
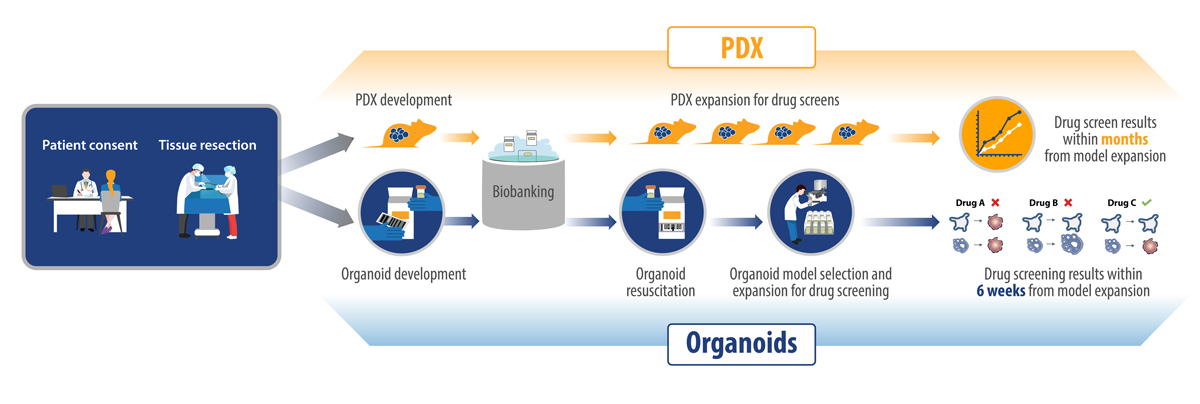
精准医疗在肿瘤学领域的应用越来越多,用于帮助特定患者选择最佳疗法。虽然 人源肿瘤异种移植模型(PDX)具有一定的精准医疗前景,但它们尚待时间来开发,成本可能很高,且不容易规模化应用。
由于类器官肿瘤也是人源模型,因此它们与PDX非常相似,保留了原始肿瘤特征和患者的相关性,并能预测患者对治疗的反应。相较于PDX,肿瘤类器官在落实精准医疗方法方面还有其他一些优势 — 它们的开发速度更快,更容易量产。
利用肿瘤类器官可以对多种潜在治疗方式进行测试,而这些治疗方式中有很多可能并非相关适应症的标准治疗方案。可以将测试结果与其他检测(如基因组筛查)结合,从而确定耐药机制或替代治疗方案。
这类研究的典型工作流程为:
- 使用从初次治疗或既往治疗失败的癌症患者中获得的活检标本建立人源肿瘤类器官
- 建立和扩大肿瘤类器官培养
- 使用肿瘤类器官和化疗、放疗等多种抗癌治疗(单独或联合)进行体外筛选。
- 将实验室研究结果告知临床医生
对比体外类器官和患者反应时,需要做一些技术和转化方面的考量。首先,并不是所有的肿瘤都能开发成类器官 — 例如,低级别肿瘤来源的类器官转化率较低。
此外,还优化了上皮的类器官培养条件,因此,除非自体免疫细胞和基质也可用,否则无法评价肿瘤微环境对肿瘤治疗反应的作用。自体类器官和免疫细胞共培养目前正在研究中,但尚初早期阶段。要想应用于患者反应评价,仍需优化针对多种肿瘤和免疫细胞类型的方案。
使用肿瘤类器官的临床试验
利用肿瘤类器官结果作为依据的临床试验主要分为两大类:
- 指导患者选择治疗方案。在这些试验中,从癌症患者中建立肿瘤类器官,并用药物敏感性数据实时指导这些患者选择治疗方案。根据肿瘤类器官药物敏感性数据设计治疗方案。
例如,一项即将进行的创新性临床试验( ORGANOTREAT-01试验,由巴黎的Gustave Roussy/INSERM开展)提出,使用类器官得到患者的个性化化学成像图,找到他们预想不到的治疗方案。当晚期结直肠癌等消化道癌症患者行将完成最后一道治疗时,将对其进行活组织取样检查。
然后使用产生的人源肿瘤类器官对一组(26种)治疗进行检测,以评价6周内的抗肿瘤活性,并尽快给出其他或替代治疗建议。次要目的是评价根据化学成像图接受治疗的患者的比例以及不同治疗方案的疗效。 - 为具有相同肿瘤特征的后续患者推介治疗方案。在这些试验中,患者及其来源的肿瘤类器官接受相同的药物方案治疗。然后将临床结果与肿瘤类器官的药物敏感性数据进行对比。这些研究的主要目标是使用下游数据,为后续具有相同肿瘤特征的患者推介治疗方案。
最近的一项联合临床研究开发了转移性结直肠癌类器官,用于评价类器官相比来源患者的药物反应。在靶向药物治疗和化疗中,类器官的阴性预测值为100%,阳性预测值为89%,证明了肿瘤类器官的临床相关性。
结论
人源肿瘤类器官由于忠实再现了亲代肿瘤的复杂性,且适合快速、多试剂检测,因此被看作是一种改变癌症精准医疗的新方法。这些正在进行的临床试验将验证肿瘤类器官对精准医学的适用性,从而为患者治疗提供指导。