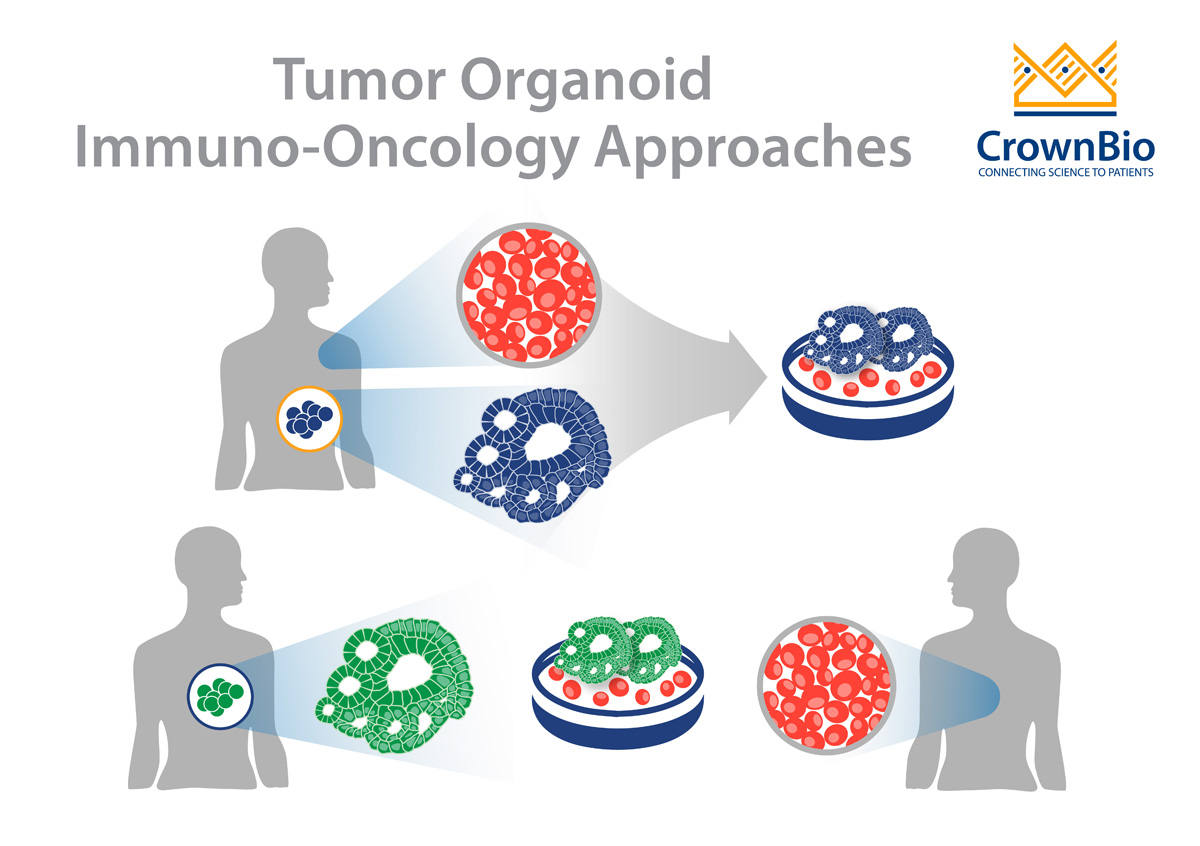
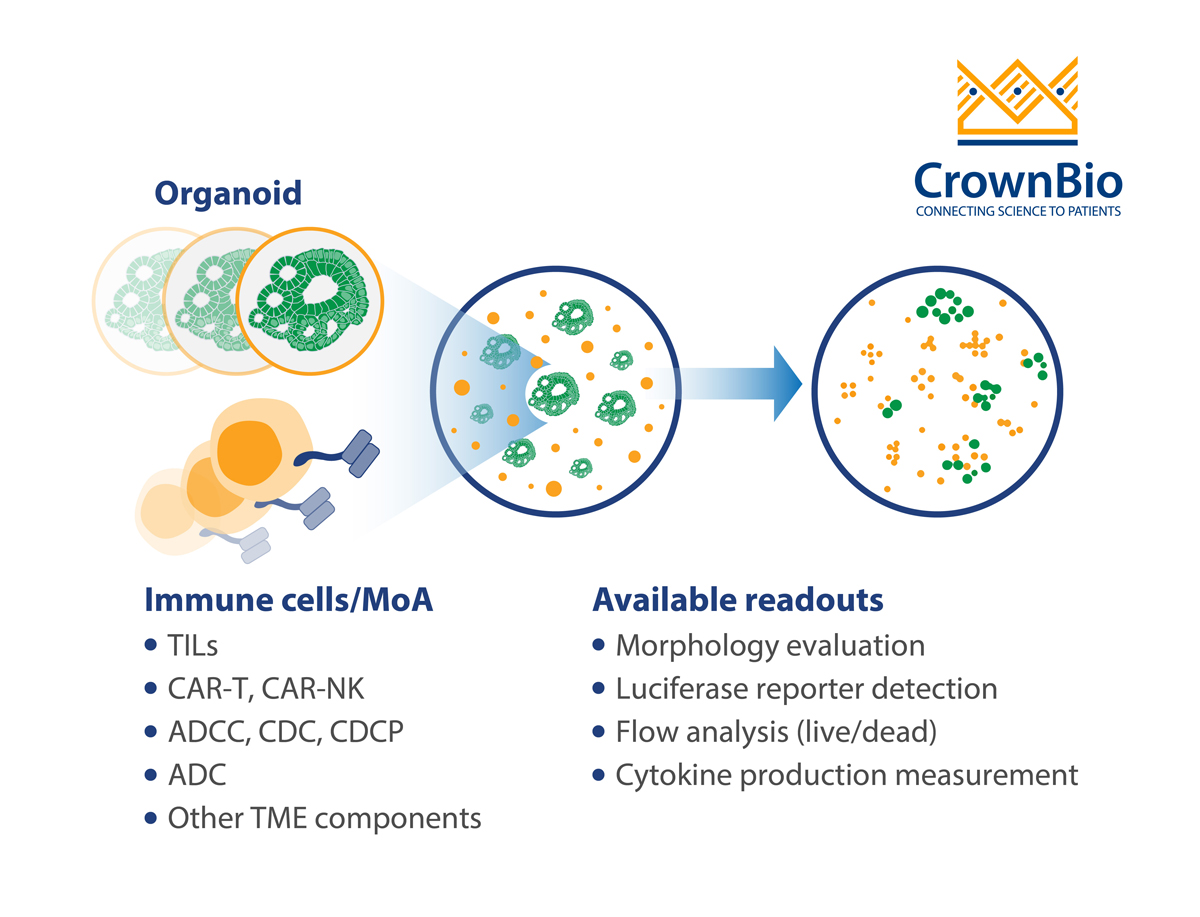
探讨肿瘤类器官在肿瘤免疫学中的应用,包括通过与自体和非自体免疫细胞共培养进行免疫治疗评估。
免疫治疗药物研发面临的挑战
众所周知,癌症免疫疗法的体外测试是具有挑战性的。这是由于I/O药物需要肿瘤和免疫系统之间复杂而动态的相互作用,而这些相互作用只有在体内才能完全再现。
然而,现有的体内I/O模型也远非完美。目前的免疫肿瘤模型面临着共同的挑战,包括
- 种属特异性:尽管同种移植模型具有强免疫系统,但它们只能用于评估交叉反应或代用品
- 人源化体系的复杂性,导致研发成本高,周期长
- 移植物抗宿主反应限制了实验窗口
- 供者与供者之间的差异可能使数据解释复杂化
- 免疫系统的部分或无效重组建,限制了I/O模型对针对非重建部分的测试品的适用性
类器官共培养在I/O 的应用
肿瘤类器官是直接患者组织来源体外模型,已经对非I/O药物的评估产生了革新式的进展,也成为在体外免疫治疗评估中的一个新兴工具。这些创新的由患者组织建立的三维模型具有临床相关性、人群多样性特点,可以提供患者反应的预测。
到目前为止,体外免疫治疗模型建立的主要挑战有:
- 在共培养系统中测试患者资料有限
- 自体免疫细胞缺乏抗肿瘤活性
肿瘤类器官有助于克服这些问题。它们被用于与自体或非自体免疫细胞的共培养,为免疫治疗的发展提供与患者相关的体外平台。
肿瘤类器官与免疫细胞共培养的优势
体外肿瘤类器官在肿瘤免疫学中是增强了肿瘤类器官的临床相关性(与癌细胞系相比较)。异质性的三维结构和空间排列形成了迷你器官,迷你器官可以体现原始肿瘤的基因组、形态和生理特征。有助于为I/O药物产生更准确的疗效和效力数据,确认耐药机制或了解治疗失败的原因,了解模型多样性/异质性。
类器官共培养平台的体外特性也使它们比体内模型更具可扩展性,这意味着可以同时测试多个药物和供体/模型组合。另一个优势在于,对应的健康的类器官也可以同时开发,以评估对人体组织的任何潜在的脱靶效应,这在体内模型是不可能实现的。
肿瘤类器官与自体免疫细胞共培养
这种实验方法涉及免疫细胞和来自同一病人(自体)的肿瘤类器官的共培养。这个共培养系统由Dijkstra等人发表,他们评估了T细胞对CRC和NSCLC类器官的特异性反应。
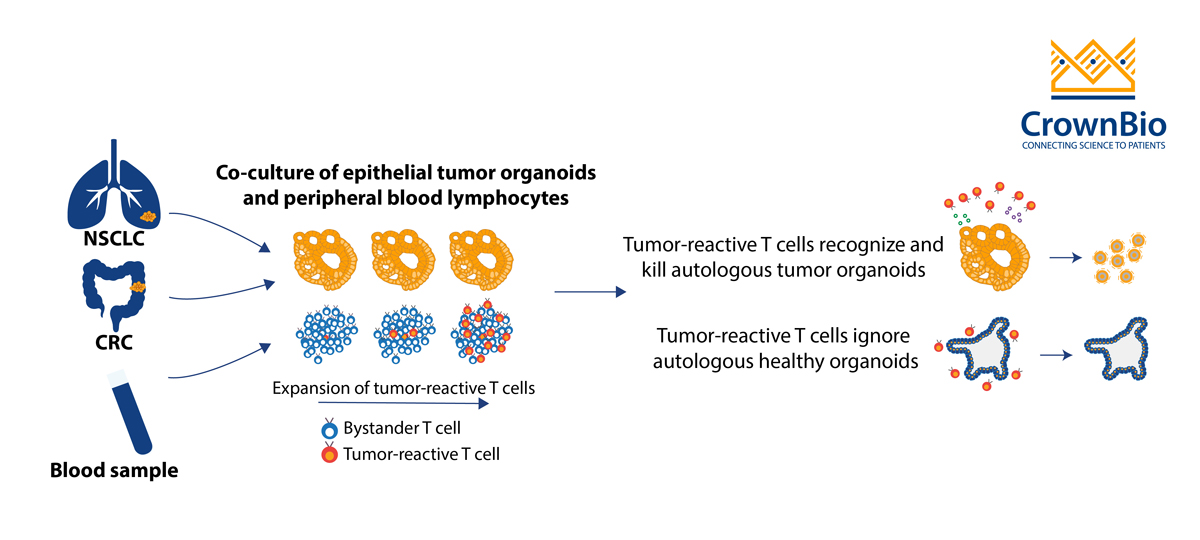
经过两周的肿瘤类器官与自体PBMCs共培养,观察到明显的肿瘤反应,CD8 + T细胞IFNγ分泌和CD107a表达上调。这些反应被证实是肿瘤特异性的,因为在与来自正常结肠或肺组织的类器官样品共培养中未检测到T细胞的反应活性。形态学和生物标志物分析也表明,扩增的自体反应性T细胞能有效地杀伤肿瘤类器官。
肿瘤类器官与自体免疫细胞共培养的挑战
自体PBMC与肿瘤类器官共培养尚处于实验室研究阶段。与这种方法相关的一些公认的挑战包括:
- 癌症患者供体可提供的血液量有限
- 大多数供者的PBMC中缺乏肿瘤反应性T细胞
- 药物研发应用中可扩展性有限
肿瘤类器官与非自体免疫细胞共培养
一种更可行的肿瘤免疫药物研发方法是使用类器官和非自体免疫细胞共培养,这种方法克服了上述的一些挑战。非自体免疫细胞更容易从健康的供体获得。在这里,不是使用匹配的类器官和免疫细胞,而是根据不同的标准选择类器官或免疫细胞。
- 根据基因或蛋白表达特性靶向选择感兴趣的或特定突变的类器官。
- 可以选择多个非自体免疫细胞供体或分离不同的免疫细胞。
肿瘤类器官和非自体免疫细胞共培养平台可以用于以下方面:
- 异体T 细胞杀伤肿瘤类器官实验以评估免疫治疗制剂的效力
- CAR-T和TCR T细胞的肿瘤类器官杀伤和肿瘤反应性
- ADCC (NK)和ADCP(巨噬细胞)杀伤肿瘤类器官
肿瘤类器官与非自体免疫细胞共培养的挑战
肿瘤类器官与非自体免疫细胞共培养也存在一些挑战,其不能检测肿瘤抗原特异性。肿瘤类器官与非自体T细胞共培养可以检测同种异体T细胞对肿瘤类器官的反应/杀伤,并检测免疫检查点抑制剂的效力。然而,在临床上,免疫检查点抑制剂的目的是提高T细胞对特定肿瘤抗原的反应,而不是诱导同种异体T细胞的反应。类器官和非自体免疫细胞平台的下一步发展应该可以检测肿瘤抗原特异性T细胞的反应性。
基因工程编辑肿瘤类器官,以开发独特的新的免疫治疗模型
肿瘤类器官在肿瘤免疫学应用中的另一个明显的优势是:与体内模型相比,可以构建特定类器官以建立新的免疫治疗模型,例如构建表达特定CAR-T靶标的类器官。这些模型也可以修饰成表达荧光素酶或荧光标记的类器官,通过成像检测对肿瘤类器官的杀伤。
结论
在肿瘤免疫学应用中使用肿瘤类器官为研究人员提供了又一个有吸引力的临床前选择,为I/O药物研发体外模拟肿瘤的复杂性。虽然肿瘤类器官和自体免疫细胞共培养还处于起步阶段,但肿瘤类器官和非自体免疫细胞共培养的新平台可规模化地应用于肿瘤免疫药物研发。这种新平台的使用可以更好地模拟个体患者,产生更多临床相关的结果。