由于缺乏靶向药物治疗方案,食管癌患者存在术后/放化疗后预后不良现象。一份新的报告详细介绍了应用临床相关PDX模型进行ESCC西妥昔单抗(cetuximab)的临床前药效评估,即评估其反应并确定候选预测生物标志物。
食管癌患者缺乏靶向药物治疗方案
即便近年来,在综合治疗和手术技术方面取得了进展,但食管癌预后仍不佳。在全球癌症相关死因排名中,该疾病名列第六,因此急迫需要新的治疗方案。
虽然针对特定致癌改变起作用的靶向药物已成功应用于许多癌症类型,但就食管癌而言,仅少数药物(如HER2抑制剂)可适用。其他研究关注了靶向VEGF / VEGFR、COX-2、mTOR和EGFR。
EGFR在食管癌中的意义
EGFR在食管癌中的作用很大,EGFR过度表达与预后不良和恶性疾病相关。此外,研究人员在食管癌亚型中也观察到不同水平的基因扩增。许多研究小组正在进行针对食管癌患者进行有效的靶向EGFR治疗。
目前,抗EGFR单克隆抗体(西妥昔单抗,帕尼单抗(panitumumab))和酪氨酸激酶抑制剂(吉非替尼(gefitinib))在食管癌和食管鳞癌(ESCC)中的应用已进入试验阶段,这两种疾病中EGFR表达过高。然而,结果差异较大而且疗效不佳,不如正在测试的对照组。
到目前为止,大多数研究已将西妥昔单抗加入到ESCC化疗/放疗中,但没有先界定一个合适的ESCC亚型,或没有使用预测性生物标志物进行反应。
应用人源异种移植(PDX)识别响应人群
人源异种移植是高度临床相关的临床前模型,该模型用于再现人类疾病。在小鼠临床试验中大量应用这些模型模拟患者II期试验。每位PDX受试者反映其源患者的病理,相当于“患者”,且 “患者”组代表人类患者群体的多样性。
除研究患者人群对药物的反应外,PDX小鼠临床试验的另一个主要用途是确定预测性生物标志物。该试验已成功测试了胃癌和结直肠癌患者对西妥昔单抗反应和生物标志物,以及SCLC患者中PARP抑制剂反应。
Zhu等人采用这种方法即,首次应用PDX小鼠临床试验研究西妥昔单抗在食管癌中的疗效并确定反应的生物标志物。
应用ESCC PDX模型进行小鼠临床试验
一共产生61个ESCC PDX,其中16被选入进行小鼠临床试验。由于处于不同分化水平,它们涵盖了多个疾病阶段。
所有入选模型均进行广泛表征,以便将反应与致癌特性联系起来。常见的PDX模型表征包括以下几点:
- 组织病理学分析。
- 转录组测序。
- 基因拷贝数分析。
- 蛋白表达分析。
以外,还应用数据剖析检查癌症中常见的活化致癌途径以便完全允许生物标志物测定。
小鼠临床试验可揭示响应者亚群
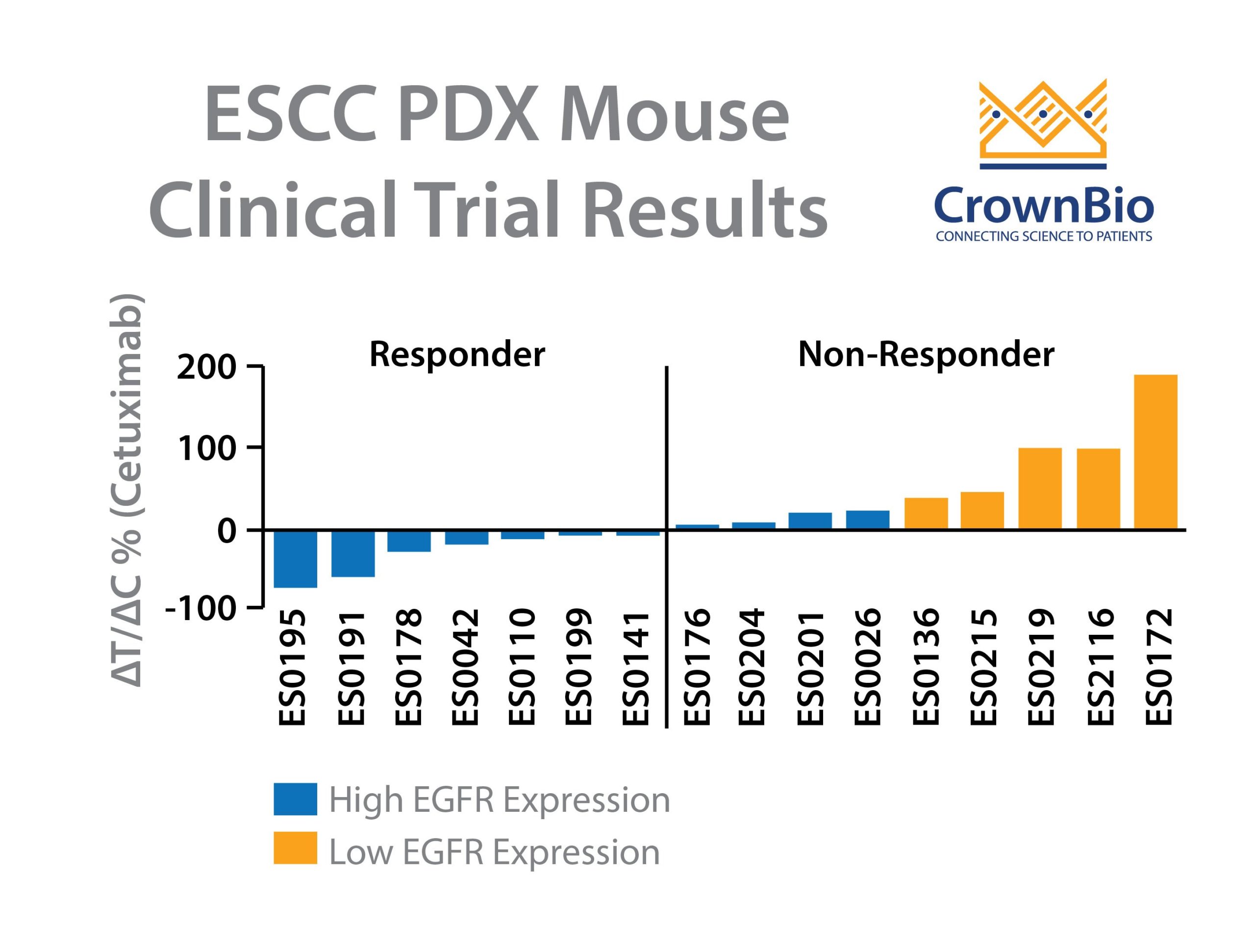
用单药西妥昔单抗治疗PDX模型并评估反应。ESCC PDX模型组明显分为两组:
- 16个模型组中有7个为响应者(ΔT/ΔC <0)。
- 其余9个为非响应者(ΔT/ΔC >0)。
在响应模型中,其中有两个几乎为完全响应,其余五个为部分响应。该小鼠临床试验数据清楚地表明,西妥昔单抗治疗对部分ESCC患者有疗效。
EGFR表达正向预测了西妥昔单抗反应
然后,结合反应和表征数据,研究小组便可开始挑选预测性生物标志物。由于西妥昔单抗结合表面表达的EGFR,因此,EGFR状态为首个起点。
首先,测定EGFR拷贝数。结果发现其扩增率为37.5%,与西妥昔单抗反应显着相关。接着,评估EGFR mRNA水平,结果显示所有高表达者皆为西妥昔单抗响应者。最后,检测EGFR蛋白水平,结果显示EGFR和pEGFR的高IHC评分也与肿瘤反应相关。
上述分析表明EGFR可作为ESCC患者对西妥昔单抗反应的单一预测生物标志物。另外,研究人员还评估了其他癌基因及其下游效应分子(如MET、HGF、ERBB2、AKT),但似乎没有一种可作为预测西妥昔单抗功效的有前景的备选生物标志物。
总结
食道癌治疗领域非常需要靶向药物来提高患者的存活率。将预测性临床前模型应用于小鼠临床试验可进行肿瘤反应分析并确定预测性生物标志物。
研究人员从该类型的ESCC化身试验中发现一种EGFR拷贝数、mRNA和蛋白质水平过度表达的疾病亚型,该亚型患者人群可从单药西妥昔单抗治疗中获益。这些数据有望得到临床证实且可能是这种恶性疾病的新疗法。
更多详情
Zhu 等人。通过EGFR高表达和扩增预测,对西妥昔单抗有反应的食管鳞癌患者源异种移植亚群。《胸部疾病期刊》2018;10(9):5328-38。