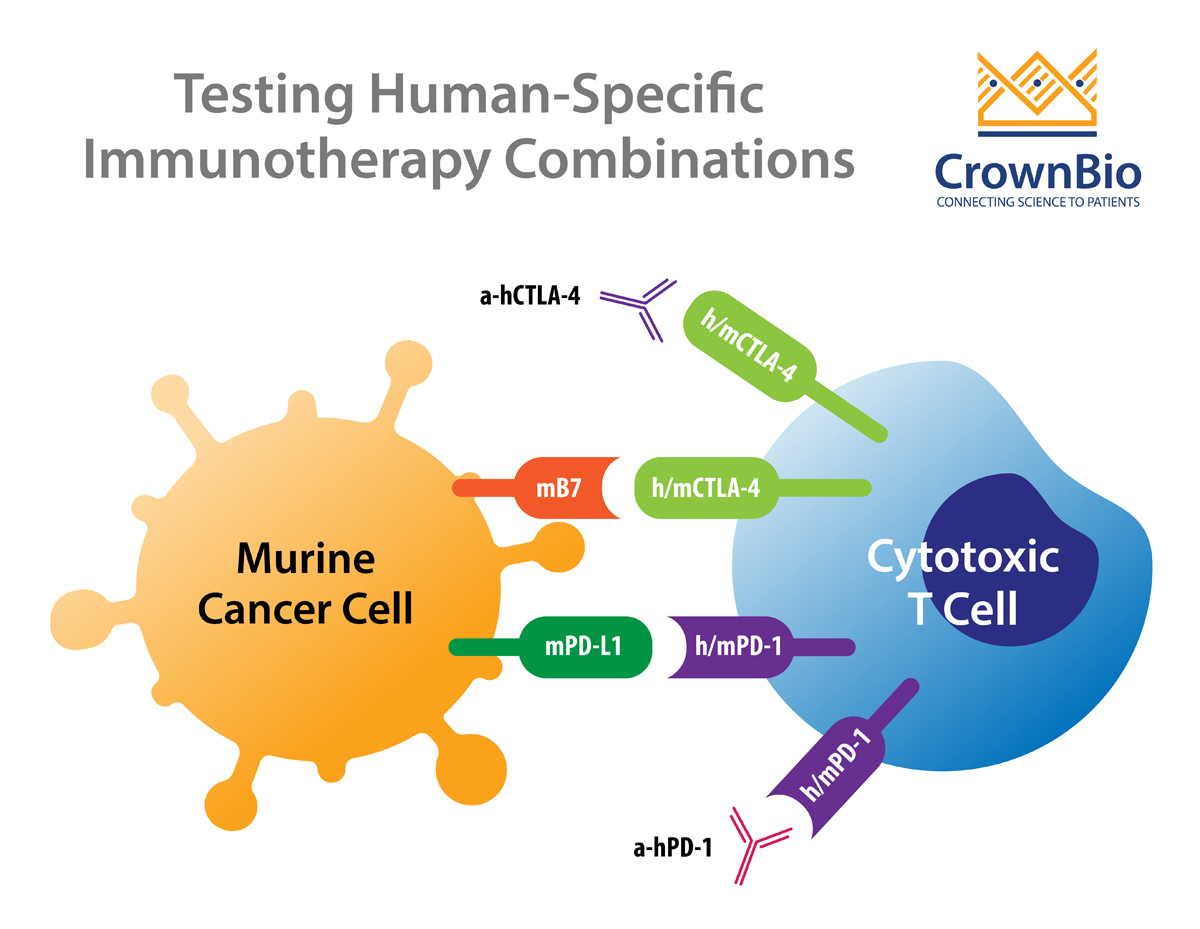
了解如何利用双基因敲入的药物靶点人源化小鼠模型评估人类特异性检查点抑制剂的体内联合疗法。
试验联合免疫疗法
联合疗法结合了其它肿瘤免疫学药剂和靶向治疗,是免疫治疗的未来走向。为了评估这些体内联合疗法,需要有适用模型。
对于鼠源药剂,目前可用同基因或小鼠肿瘤同种移植之类的模型。但对于人源特异性疗法,由于品种的特异性问题,这些鼠源模型就被排除在外。
现在有了新的临床前模型,专门设计用于评估靶向常见检查点蛋白的人类特异性药剂的体内联合疗法。这类模型具有双药物靶点人源化(如人源化PD-1和CTLA-4)的特点,同时具有健全的小鼠免疫系统。
药物靶点人源化模型
在探讨双基因敲入模型之前,最好先回顾,引入单基因敲入药物靶点人源化模型(双基因敲入模型由此培育而来)的概念。
小鼠模型作为一个强大平台而存在,各个模型都具有人类肿瘤免疫靶点基因稳定表达(如PD-1、CTLA-4、OX40、CD40等)的特点。这类模型经过基因工程改造,把以待研究的小鼠基因换为人类基因。
然后对模型进行高度表征,在适用免疫细胞群中确定人类检查点蛋白表达,并加以验证,保证模型对人源抗体有反应。
这样就生成一系列具有活性免疫系统的模型,这类模型主要用于评估人类特异性检查点抑制剂,或免疫系统靶向激动剂抗体。这类模型对下述早期阶段研究最为理想:
- 验证治疗性抗体在体内结合正确靶点。
- 排除最终来自药物治疗的毒性。
药物靶点人源化模型对“标准”临床前疗效研究也大有益处。在这类研究中,随着时间的推移,评估对照组和治疗组的肿瘤负荷,计算药剂对肿瘤生长抑制的百分比(TGI)。
联合治疗方案虽可评估,但仅限于一种人类特异性药剂和一种小鼠模拟药剂(例如,在PD-1人源化模型中检测人源PD-1和鼠源OX40)。
培育双基因敲入模型
当需要评估两种人类特异性药剂联合疗法时,需用双基因敲入模型。这类模型在同一免疫活性小鼠内具有两个人源化的检查点蛋白。现有PD-1和CTLA-4、PD-1和PD-L1、PD-1和OX40的双基因敲入模型,其它模型正在验证中。
双基因敲入模型是通过2个单基因敲入模型培育获得。以PD-1/CTLA-4双基因敲入模型为例,它是通过PD-1人源化小鼠和 CTLA-4人源化小鼠培育获得。与单基因敲入模型类似,对双基因敲入模型进行表征以确保2种蛋白质都表达。另外还要进行单药剂和联合疗法的验证,在PD-1/CTLA-4双基因敲入模型中已得到一些令人关注的结果。
PD-1/CTLA-4双基因人源化模型中的免疫记忆反应
PD-1抗体和CTLA-4抗体联合治疗,使小鼠在植入表达人类PD-L1的MC38肿瘤细胞之后肿瘤完全消退。被“治愈”的小鼠于分组后数日处于无病状态,接下来被用于“rechallenge”研究。与对照组相比,再次植入相同的MC38肿瘤在被“治愈”的小鼠中会引起免疫记忆反应,未见新肿瘤生长。
综上所述,该模型具备功能小鼠免疫系统,表达2个人源化药物靶点基因,适用于体内检查点抑制剂联合疗法试验。
结论
我们通过新联合疗法来扩大免疫治疗反应,需要更多的临床前模型开展人类特异性药物的体内研究。双基因敲入的药物靶点人源化模型,可用于评估最常见的人类特异性检查点抑制剂的联合疗法,也为更复杂的完全人源化模型提供了更具成本效益的替代方案。