在本文中,我们探讨了如何将靶向RNA测序(RNA-Seq)组纳入临床前药物开发,以评估免疫效应物在辅助新型免疫肿瘤学(I/O)药物抗肿瘤免疫中的影响。一项病例研究强调了RNA-Seq组如何补充传统的基于蛋白质的分析,以获取有关新型免疫疗法的真正全面的图片。
精准医疗:承诺与挑战
 检查点阻断以及其他形式的癌症免疫疗法可以对越来越多的癌症适应症产生持久的临床反应。值得注意的是,在既往无有效治疗方法的多种晚期癌症中观察到这种反应。
检查点阻断以及其他形式的癌症免疫疗法可以对越来越多的癌症适应症产生持久的临床反应。值得注意的是,在既往无有效治疗方法的多种晚期癌症中观察到这种反应。
然而,与其他抗癌治疗类似,仅一部分患者受益于增强抗肿瘤免疫的治疗。这引起对识别新型生物标志物的迫切需要,以识别最有可能对免疫治疗有反应的患者。
理想情况下,此类生物标志物应包含肿瘤微环境(TME)的特征,因为众所周知,肿瘤微环境中免疫细胞的组成和密度会深刻影响肿瘤进展和抗癌治疗的疗效。
对肿瘤微环境进行基因组分析,在改善当前和新型免疫治疗方案方面发挥着越来越重要的作用。
肿瘤微环境定性分析
高通量RNA-Seq已经彻底改变了癌症基因组学,并为获取肿瘤微环境的复杂分子特征和相互作用提供了一个有前景的途径。
到目前为止,基于蛋白质确定的方法,如荧光激活细胞分选系统(FACS)、免疫组织化学(IHC)和免疫荧光法(IF)被认为是估计样本中免疫细胞含量的金标准。
虽然这些技术仍然可以提供有价值的见解,但这些方法存在技术局限性,其应用无法更广泛。例如,一项针对潜在蛋白质生物标志物的高质量经验证抗体可用性或缺乏性的连续性挑战。
此外,IHC和IF以及在较低程度上的FAC在可同时检查的标志物数量上受到限制(与不同方法相关的一些常见局限性见表1)。
表1.用于肿瘤微环境量化分析的方法。
| 方法 | 局限性 |
|---|---|
| FACS | 需要大量材料,标志物数量有限 |
| IHC / IF | 如果肿瘤具有异源性且标志物数量有限,则不具有代表性 |
| RNA-Seq | 不提供有关细胞组成的信息 |
| sc-RNAseq | 由于组织分离,价格昂贵且存在偏倚 |
新一代RNA-Seq是蛋白质技术强有力的高通量替代或补充方法,在无需预先选择特定靶点的情况下,精准测量整个基因组中的基因表达。
此外,从RNA-Seq获得表达量化和核酸序列信息的能力可用于测量免疫信号,这些信号通常凭借多种不同技术获得。
随着单细胞RNA测序技术(sc RNAseq)的进展,肿瘤细胞与肿瘤微环境的复杂相互作用现在可以得到精确重建。这些好处可以降低成本,可帮助研究人员能够在最后期限前完成或快速跟踪项目。
需要基于小鼠新一代测序(NGS)的分析作为临床前药物开发的基本工具
描述肿瘤微环境的基于RNA的分子特征的预后价值已在最近的临床试验中得到证实,其中肿瘤浸润免疫细胞的基因表达特征已在几种恶性肿瘤中产生。
但这种类型的评估不必局限于药物开发的临床阶段。
相反,在进入人类临床研究之前,应该更好地了解肿瘤微环境在免疫治疗的作用机制(MoA)和疗效中发挥的作用。
通过使用在药物开发过程早期提供了解肿瘤微环境的分析,以及适用于免疫肿瘤学研究的一系列临床前模型,我们旨在改善患者分层,以提高新型制剂的疗效和安全性。
小鼠免疫肿瘤学靶向RNA-Seq组 (称为小鼠I/O RNA-Seq组)可用于评估与肿瘤免疫相关的基因。该评估将对肿瘤微环境中的关键免疫细胞系和免疫肿瘤学通路和过程(图1)进行快速转录组学深入分析。
例如,在一项包含1080个基因的小鼠I/O RNA Seq可用组中,可以分析免疫细胞特征、表面标志物、转录组免疫细胞特异性生物标志物以及肿瘤、肿瘤微环境和免疫应答界面处的关键通路。
图1:小鼠I/O RNA-Seq组的定性

小鼠I/O RNA Seq组的典型工作流应设计简单,并在可分析的研究样本的来源和类型方面具备灵活性(图2)。
工作流具备灵活性至关重要,以至于通过
同源和MuPrime研究、内部研究或外部生成的样本生成的样本(例如,提取的RNA、冷冻组织、全血、免疫细胞颗粒)可以无缝集成到工作流中。
最后,最终输出应包括原始数据和标准化数据,以及一份包含多组/条件比较的综合报告。
小鼠I/O RNA Seq组也适用于大规模筛选研究 (如MuScreen 体内药理学平台)。
大规模筛选研究利用一系列经验证的同源和肿瘤同种移植物模型,涵盖多种癌症类型和免疫特征,为研究人员实现以下独特内容:
- 深入了解制剂的MoA
- 识别可能预测应答的生物标志物
- 使用与人类有关癌症相关的临床前模型
图2:小鼠I/O RNA-Seq组工作流的特点。

与其他常用转录组学技术相比,RNA-Seq平台有一些优势(这两种分析的比较见表2)。
RNA-Seq与Nanostring的比较研究 (一种基于DNA的微阵技术的变体)表明,小鼠I/O RNA-Seq组的准确度和灵敏度更高,能够区分不同的小鼠品系,周转时间更短,因此更具成本效益。
表2.平台比较:小鼠I/O RNA-Seq组 vs 基于微阵列的免疫肿瘤学分析
小鼠I/O RNA Seq组可以补充和增强基于荧光激活细胞分选系统(FACS)的免疫肿瘤学分析
| 分析方法比较 | ||
|---|---|---|
| 小鼠I/O RNA-Seq组 | 微阵列免疫肿瘤学分析 | |
| 技术 | 靶向深度NGS | 靶点mRNA(cDNA)与DNA探针混合 |
| 靶分子 | mRNA | mRNA |
| 通量 | 高(1080个基因) | 高(数百到数千个基因,视供应商而定) |
| 准确度 | 高 | 低-中 |
| 检测低表达基因的灵敏度 | 高 | 低-中 |
| 小鼠品系区分 | 是 | 否 |
| 周转时间 | 2-3周 | 3-10周,视供应商而定 |
| 成本 | 低 | 中度 |
Mouse I/O RNA-Seq panels can complement and enhance fluorescence-activated cell sorting (FACS)-based I/O profiling
如上所述,RNA-Seq克服了基于蛋白质的肿瘤微环境分析方法的一些关键局限性。除了靶分子的差异外,与FACS相比,使用小鼠I/O RNA Seq组具有更高的通量(高达1080个靶点 vs 约30个靶点),更高的准确度,并且适用于大规模样本筛选。
此外,小鼠I/O RNA Seq组可以用作发现工具,而FACS最适用于假设检验和验证。
与一些基于蛋白质的方法相比,RNA-Seq组的公认局限性是周转时间较慢,但RNA-Seq平台确实提供了更全面的样本分析,每个样本的成本相对较低(RNA-Seq组的优势见表3)。
此外,值得注意的是,小鼠I/O RNA-Seq平台不一定取代基于蛋白质的分析方法,但在获取有关肿瘤样本中免疫细胞含量和效应物通路激活的最完整信息方面,可以将其视为一种辅助工具。下面的病例研究强调了这种辅助方法的效能。
表3.小鼠I/O RNA-Seq组优势总结
| 小鼠I/O RNA-Seq组优势 | |
|---|---|
| 综合性 |
|
| 灵活的样本类型 |
|
| 高通量 |
|
| 高灵敏度 高准确度 |
|
| 易于整合 |
|
| 成本效益好 周转快 |
|
病例研究:测定不同饮用水pH下的免疫治疗反应
许多研究表明,在动物模型和人类中,肠道微生物群(GM)在免疫治疗反应中起着重要作用。已知体内临床前变量,如饮食、住房、床上用品和饮用水的pH值(如研究设施中常用的酸化饮用水)会影响GM。
然而,这些变量对免疫治疗反应的影响尚不清楚。因此,本研究使用靶向RNA-Seq和FACS作为补充数据源,研究了饮用水pH值对MC38小鼠结肠癌模型抗PD-1疗效的影响。
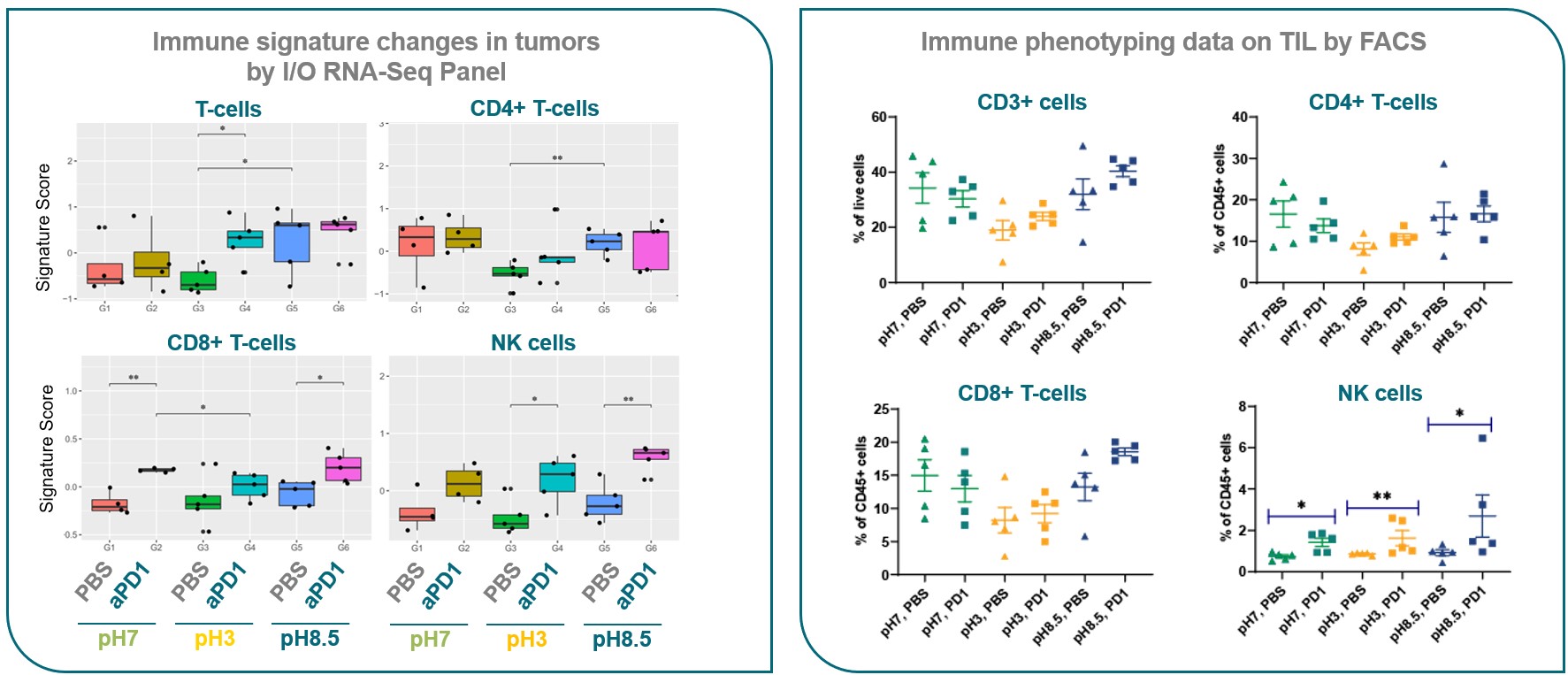
MC38肿瘤的RNA-Seq分析与FACS数据一致,证实接受酸化水的小鼠总淋巴细胞浸润(CD45+)、T细胞(CD3+、CD4+和CD8+)最低,NK细胞百分比最高。
这些结果表明,酸化水可以通过诱导免疫抑制肿瘤微环境来调节免疫治疗反应(图3)。
图3:抗PD-1治疗以及给予不同pH水平饮用水后MC38肿瘤的免疫特征(RNA-Seq)和免疫细胞表型(FACS)分析。
利用小鼠I/O RNA Seq组所覆盖的免疫特征的增加数量,通路分析显示低氧、MAPK和TGF-β信号也受到pH值的影响,碱性条件促进抗原呈递。
图4:抗PD-1治疗后给予不同pH水平的饮用水对MC38肿瘤的免疫特征分析

在研究的疗效部分,对MC38和CT26.WT结肠癌模型进行了评估。研究发现,饮用水的不同pH水平对MC38模型的抗PD-1疗效的影响更显著。
具体而言,该模型中的抗PD-1治疗显示,碱性水(TGI=74%)的肿瘤生长抑制作用最大,其次是pH中性水(TGI=66%),然后是酸化水(TGI=58%)。
图5:不同pH水平饮用水对MC38和CT26.WT小鼠结肠癌模型抗PD-1治疗的反
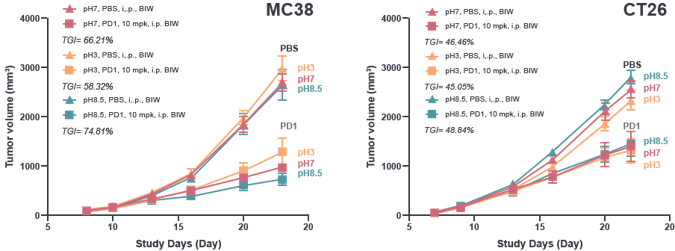
综上所述,中性至碱性水可导致免疫效应细胞的扩张,抑制肿瘤抑制亚群,激活促进抗肿瘤免疫的信号通路。
根据这些数据:
- 建议在采用同源小鼠模型的临床前免疫肿瘤学疗效研究中使用碱性水
- 在探索旨在增强肠道微生物组的治疗方法时,也应提供碱性饮用水
- 在进行免疫肿瘤学研究时,应避免使用酸化水,因为它可能通过调节微生物群落削弱对治疗的反应
结论
利用RNA-Seq组为研究人员提供了多种独特优势,以补充传统的基于蛋白质的分析。总之,这些分析有助于精确定位作用机制(MoA),并识别可能改善新免疫治疗剂可转化性的可预测性生物标志物。
通过在开发早期加入能够充分定性肿瘤微环境的策略,研究人员有最好的机会加速免疫治疗研究,并为临床成功定位。
有关小鼠I/O RNA Seq组的更多信息,请查看我们最新的按需网络研讨会。