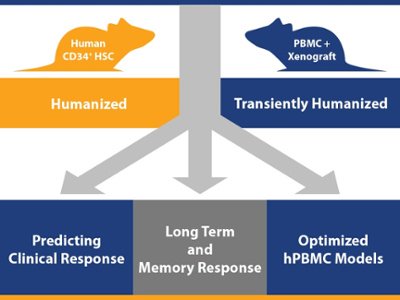
最近,我们一直关注人源化小鼠模型,从免疫缺陷小鼠的演化到衍生型hPBMC和hCD34 + HSC人源化小鼠的发展,我们均有所探讨。这篇文章将介绍如何将人源化小鼠与人类肿瘤相结合,从而在人类特异性免疫治疗药效研究中发挥3个重要用途。
1. 使用优化的hPBMC模型进行有效的药效实验
研究结果表明,荷瘤的人源化小鼠是人类特异性免疫治疗药效研究的关键。 我们要做的重点是优化模型以进行更高效的研究。
如果想要使用人源化模型和人类肿瘤组合直接进行简单的药效实验,最好的方案是使用hPBMC模型——可以从市场上获得免疫细胞,然后建立PBMC模型,有很多T细胞和NK细胞靶点可以进行测试(包括检查点抑制剂),而且相比hCD34 + HSC模型,hPBMC模型的成本更低且操作更简单。
但有两个缺点需要克服,其一是需要进行有效的研究 ,由于供体之间的差异性以及移植物抗宿主疾病(GvHD)的发生,因此需要优化模型。
使用两种不同的供体来克服差异性
在仔细设计研究实验的情况下,hPBMC模型可以克服部分供体之间的差异。 由于来自不同捐献者的人源化小鼠模型的药效均不同,因此在每项研究中通过使用来自至少两个不同捐献者的PBMC,可以解决供体差异问题。
在研究开始之前,优化每一个肿瘤模型和细胞供体联合接种方案
优化实验方案可以克服GvHD的发生。 hPBMC模型在免疫细胞移植后2-3周开始发作GvHD,第4周左右开始严重发作,这意味着需要在很短的治疗窗口期内进行药效实验。
首先,异种移植模型首选细胞系接种(CDX),因为它们生长快速。 接下来,对于每种肿瘤模型和细胞供体组合,需要调整接种方案。 此时,需要达到一个良好的免疫细胞重建水平,以便通过测量肿瘤大小来判断最佳肿瘤抑制,同时需要注意的是,需在植入后15-20天内进行肿瘤模型和细胞供体的结合。
各个肿瘤模型和各个细胞供体间的不同组合可以建立一系列人源化肿瘤模型,以用于体内药理学研究。例如在更复杂的人源化研究之前初步筛选药剂、在短期内得到有效数据,或进行高通量研究。
2. 研究免疫疗法的长期药效和记忆反应
为了达到免疫肿瘤学中理想的长期抗肿瘤效果,还需用小鼠模型进行临床前试验。 此外,在免疫疗法治疗后患者的长期无病生存率与记忆反应之间的关系也需要通过进行实验来解释。
长期模型需要免疫系统多谱系分化
由于这些研究需要长期运行,因此排除了有GvHD反应的hPBMC模型,即必须使用hCD34 +人源化小鼠模型。 hCD34 +人源化小鼠对于长期研究很有用,这些模型的人类免疫细胞成熟后可进行长达32周的长期药效实验,并且免疫系统的多谱系分化可以支持更复杂的研究,还可以解释更具体的反应机制问题。
PDX和传统的异种移植均可用于这些研究,由于细胞系的异种移植通常能够更快的生长且没有滞后时间,因此常被用于长期药效研究,当需要二次实验时也更多的选择CDX。
先确认模型响应,然后用肿瘤再次攻击以评估免疫系统记忆水平
在评估记忆反应之前,需要预设一些基准结果,例如异源移植肿瘤在人源化小鼠中是否生长良好(即与免疫缺陷的亲代小鼠相比是否受人源化的影响),具有抑制肿瘤生长的测试药剂对该模型是否有反应,并且这种反应是否依赖于免疫系统(即人源化小鼠模型有反应,而非人源化的则没有)。
一旦确定基准结果,并且已准备好人源化荷瘤模型,则可以用该模型进行药效评估实验。 将原始治疗组用另一批来自相同原始细胞系的细胞重新接种。 需注意的是,应与相同细胞系接种年龄的、相同细胞系批次的人源化小鼠匹配,以确定恶性细胞系。
在观察记忆反应过程中,我们期望能够观察到与年龄匹配的对照组的肿瘤生长未受抑制,而原始组在没有进一步治疗的情况下,能够抑制之前的一些肿瘤生长,这表明发生了记忆性T细胞应答。
综上所述,这项研究证实了hCD34 +模型是检测免疫疗法长期抗肿瘤作用的优秀模型,随着免疫疗法的不断发展,这将是非常有用的。
3. 使用人源化PDX模型预测临床反应
人源化肿瘤模型的第三个关键用途是预测临床反应,这需要考虑供体差异性。 我们在之前的文章中详细讨论了这一点。
群体研究将测试多个干细胞供体及多种肿瘤模型。 每个模型+供体都是一个独特的组合,因此仅针对一个供体测试多种模型,便可得到大量结果。这能够反映出小规模的临床试验。
通过群体研究克服药效反应和免疫供体的差异性
这些实验对于研究和克服反应中的差异性很重要,差异性在临床上广泛存在,并且受到每个受试者的免疫状态的影响。 使用这种特殊设定的研究方案(考虑动物和免疫细胞供体的数量),特别是使用了人源化PDX模型(能更精确地概括患者肿瘤并反映出患者群体中的响应变化),能够克服使用单个供体测试免疫疗法引起的限制 ,并预测临床药效(以及统计学上的有效结果)。
根据产生的结果可以分为反应组和非反应组,以及找出有响应的生物标志物。不同患者分别制定不同的方案,这有望改善供体筛选并最终在临床取得成功。
免疫肿瘤学中人源化小鼠模型的多种用途
目前仍有许多尚待解决的免疫治疗问题,临床前模型还需要继续开发、改进和完善以解决这些问题。 hPBMC人源化小鼠和hCD34 +人源化小鼠为解决临床前免疫疗法药效评估等一系列问题提供了十分有效的研究平台。