免疫疗法为癌症病患提高了生存机率,但也为肿瘤药物研究带来了不少困扰,因为比起一般的化学疗法或标靶药物,评估免疫疗法药剂的方式更加困难的。研究员需要有完整免疫系统的临床前模型 (或新型药剂是能够符合需求),因此同源模型又再次重回台面上。
同源模型存在的时间比细胞源和人源性动物模型更久,从研发至今至少有五十年的历史,有些是从基因改造小鼠模型(Genetically Engineered Mouse Model, GEMM)和自发性肿瘤模型中衍伸出来的。
无限增殖的小鼠癌症细胞株与同系繁殖的老鼠品系
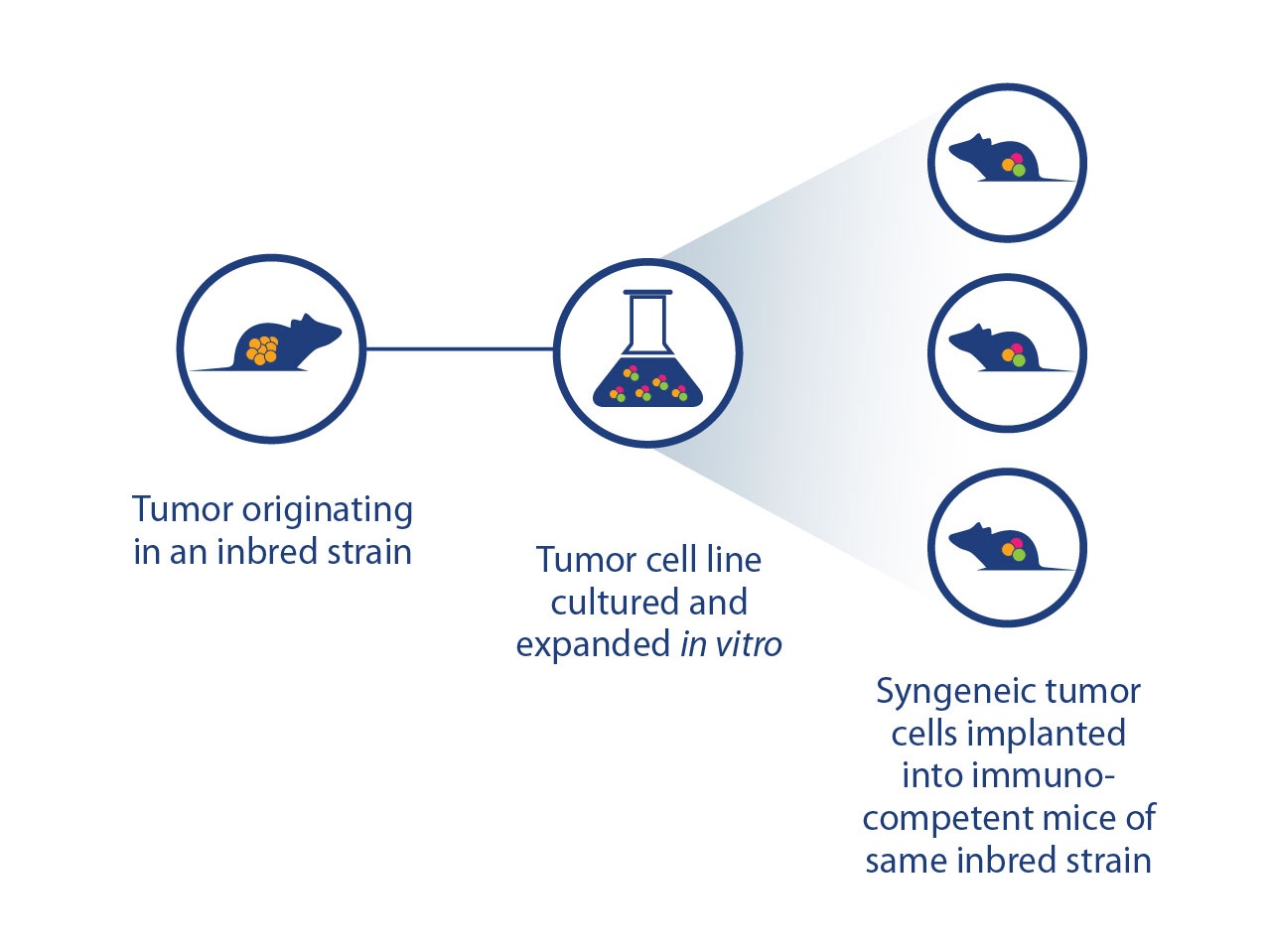
同源模型是一种能无限增殖的同种异体小鼠癌症细胞株,再将它移植到同系繁殖的免疫活性老鼠品系中。若能将可辨识的宿主与细胞株对应,便代表着肿瘤排斥不存在,因此制作出帮助免疫疗法评估的免疫活性模型。
同源模型曾经被大量使用,但肿瘤研究渐渐地往人体蛋白发展,人源性异种移殖这时候的出现成功变成肿瘤研究的主流模型。而免疫疗法的崛起,也让差点消失匿迹的免疫活性同源模型重回市面。
一个既便宜,又好用的模型
同源模型主要的功能包含了免疫活性,有著鼠类健全的免疫系统以及基质。另一个原因则是同源模型比起其他免疫活性模型(GEMM、人源化小鼠)更简化、容易理解。
同源是最能够展现异种移殖研究的免疫活性模型,也可以轻易地在任何的实验室里培养。这个模型有百分之百的外显率,皮下注射可以和肿瘤成长同步,也可以模拟异种移殖的研究设计。让研究员在极短的时间内(二至四周)得到测试结果,经济又实惠。
使用同源:联合治疗
同源模型在免疫疗法评估中有一些重点使用方法,第一种就是联合治疗,主要用的是检查点抑制剂。同源模型可以依照需求来广泛的使用,例如细胞株和肿瘤RNA定序、免疫分型、生物标记辨识,前述数据可以结合检查点抑制剂(anti-PD-1, PD-L1, CTLA-4)得到的体内效果基準成果。
集成上述所说的,这些数据提供的数据能够帮助结合疗法选择适合的模型与剂量。
同源模型平台能够快速审核免疫疗法
同源模型平台可以透过大规模筛检来快速审批免疫疗法与结合方案。正常来说,试管筛检便宜且能够快速找到未来研究需要的细胞和模型。但若融入了复杂的免疫系统,筛检较容易失败,而换成体内研究又会太贵。这时候一个大规模、符合需求的同源平台,加上适当的载具,就可以提供一个快速又符合经济成本的筛检方法。
转移性模型也适用于生物发光同源
最后原位生物发光同源也发展到了能够用在转移性模型上。这些模型可以提供这些功能:模拟及时的转移性入侵、次要器官病变、疾病末期发展、以及评估治疗转移性疾病的新型药剂。
同源模型种类的限制
所有模型都有缺点,即使像是同源这样好用的模型也有它的限制。
第一点是细胞株使用的数量。即使一个同源模型平台有超过三十种以上的模型,还是远远少于像是人源性异种移殖模型能提供的数量。在特定的癌症种类(以肺癌来说) 的表现也是不足的,也不是所有模型种类都有提供。
只适用小鼠生物学
另一项同源模型好用的原因同时也是它的缺点,因为免疫系统也只属于那只实验鼠(包含生物学和基质)。因此老鼠免疫系统的反应是否能直接应用在人类免疫系统上则成为了一大难题。
同源的研究成果不断的在产生变化
最后,即使这模型相对的稳定,每次研究成果都不一定有一样的结果。差异性的原因尚待厘清,有可能是因为小鼠的微生物群、地域性、饲养方式、或是餵食的方式而造成,也评估这些会如何影响检查点抑制剂的反应。
若想了解更多同源模型与他们适用于什么样子的肿瘤免疫模型,请看这里。