使用HuGEMM™和HuCELL™人源靶点敲入模型研究与免疫疗法相关的独特免疫相关不良事件(irAE)。该平台在功能完备的鼠类免疫系统内具有人源化药物靶点,为评估人类特异性免疫疗法靶向和非靶向毒性的复杂性质提供了理想的方法。
人类特异性疗法的疗效和毒性可在同一动物中进行评估,从而确定同一物种的最佳治疗窗口,并提供快速、经济有效和可靠的数据,以指导未来的药物研发工作。
HuGEMM模型是免疫耐受的嵌合小鼠模型,经过工程改造可以表达人源化药物靶点(而非鼠类对应物),例如编码免疫检查点蛋白的基因。
| 单敲入 | 双敲入 | 三敲入 |
|---|---|---|
| B7H3 | TIGIT/PVR | CD47/Sirpα/PD-1 |
| BTLA | PD-L1/TIM-3 | CD47/Sirpα/PD-L1 |
| CCR2 | PD-L1/TIGIT | PD-1/PD-L1/CD137 |
| CCR8 | PD-L1/OX40 | PD-1/PD-L1/CTLA4 |
| CD137 | PD-L1/LAG3 | PD-1/PD-L1/IDO-1 |
| CD27 | PD-L1/CTLA4 | PD-1/PD-L1/LAG-3 |
| CD28 | PD-L1/CD47 | PD-1/PD-L1/OX40 |
| CD38 | PD-L1/CD40 | PD-1/PD-L1/TIGIT |
| CD39 | PD-L1/CD27 | PD-1/PD-L1/TIM-3 |
| CD3E | PD-L1/CD137 | PD-1/TIM-3/TIGIT |
| CD40 | PD-1/Tim3 | |
| CD47 | PD-1/TIGIT | |
| CD73 | PD-1/Sirpα | |
| CTLA4 | PD-1/PD-L1 | |
| GITR | PD-1/OX40 | |
| IL-1b | PD-1/LAG3 | |
| LAG3 | PD-1/GITR | |
| OX40 | PD-1/CTLA4 | |
| OX40L | PD-1/CD47 | |
| PD-1 | PD-1/CD40 | |
| PD-L1 | PD-1/CD28 | |
| SIGLEC15 | PD-1/CD27 | |
| Sirpα | PD-1/CD137 | |
| STING | PD-1/BTLA | |
| TIGIT | OX40/CD137 | |
| TIM-3 | NKG2A/CD94 | |
| TNFR2 | IL2RA/IL2 | |
| VEGFR2 | CTLA4/Tim3 | |
| CTLA4/OX40 | ||
| CTLA4/LAG3 | ||
| CTLA4/CD137 | ||
| CD47/Sirpα | ||
| CD40/CD137 | ||
| CD27/CD137 |
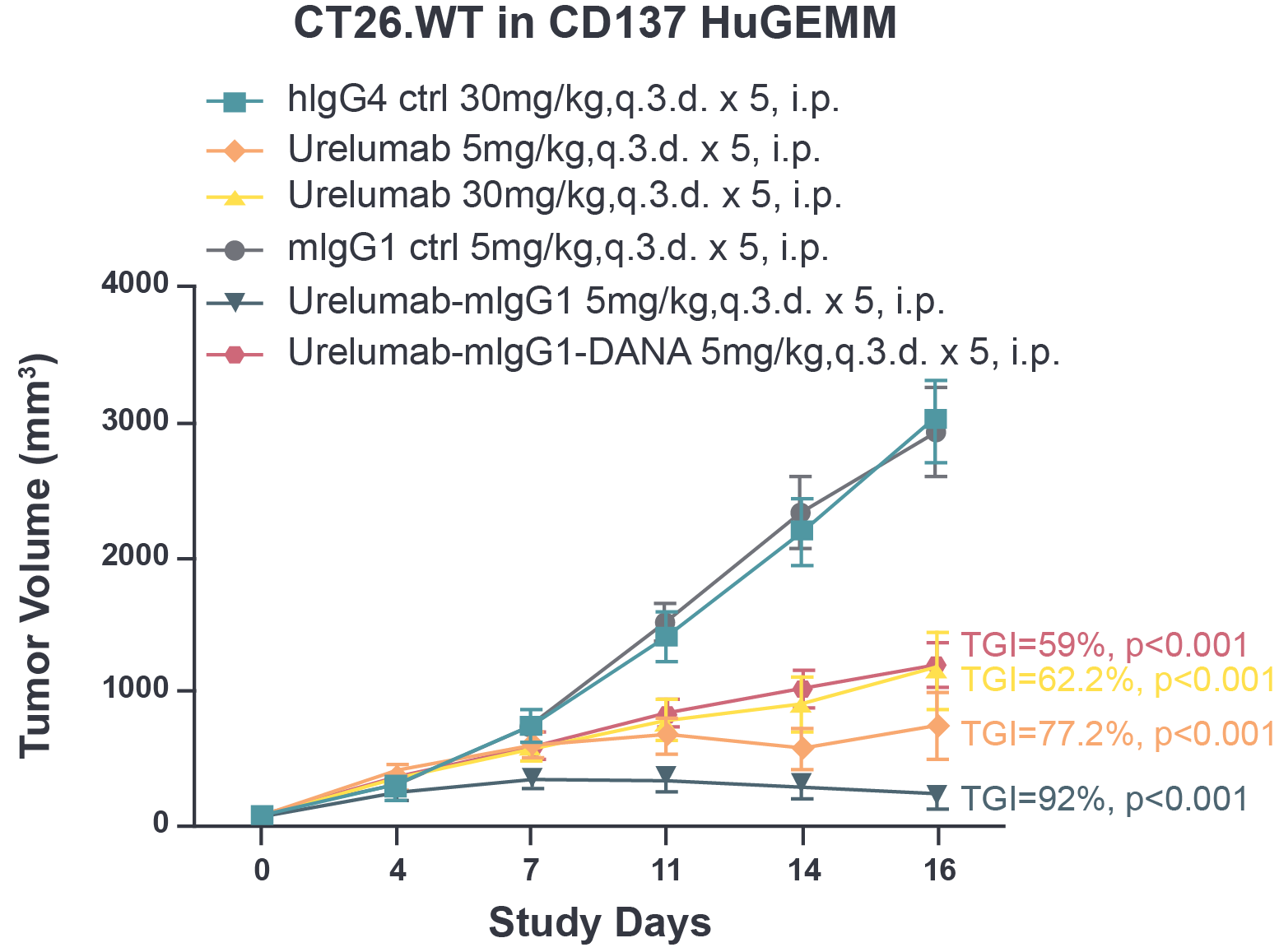
图1.在CD137 HuGEMM模型中,urelumab及其嵌合物对小鼠结肠癌CT26.WT具有抑制肿瘤生长的作用。肿瘤生长抑制(TGI的计算公式为:TGI% = (1-Ti/Vi)*100;Ti为测量日治疗组的平均肿瘤体积;Vi为测量日对照组的平均肿瘤体积。
图2.基于CD137 HuGEMM动物中的ALT(谷丙转氨酶)和AST(天冬氨酸氨基转移酶)水平来测量肝脏毒性。分别于末次给药后的第2天和第7天测量空腹血清ALT(谷丙转氨酶)和AST(天冬氨酸氨基转移酶)水平。单因素方差分析*、**和***分别表示p<0.05、p<0.01和p<0.001。
图3.在CD137 HuGEMM体内模型中,对urelumab及其嵌合物治疗后的肝炎进行组织学评估。肝组织的H&E染色。肝炎的评估等级为0-3:0=无;1=轻度;2=中度;3=重度
图4.如免疫组化染色显示,CD137 HuGEMM体内模型中,经urelumab和嵌合urelumab治疗后,CD45+免疫细胞在肝脏中的浸润情况用HALO v3.0.311.363测定。
告诉我们您的需求